作者:王晓雨 冯宏娟 杨婉婷
审校:孙超
作者单位:天津医科大学总医院消化内科
天津市第三中心医院营养科
论著链接:DOI: 10.1002/jpen.2097
研究背景
营养不良是肝硬化的主要特征之一,已被证明与较低的生活质量、较高的并发症发生率和死亡率相关。因此,欧洲肝脏研究学会(EASL)建议对所有肝硬化患者进行筛查,以详细评估其营养状况。英国皇家自由医院营养优先工具(RFH-NPT)是一种专为肝硬化患者开发的筛查工具,可以通过对容量负荷、体重波动、近期饮食和身体质量指数(BMI)等指标的评估,将营养不良进行危险分层[1]。最近的多项研究已经验证了该工具的实用性和有效性,其评估结果也被证明与各种不良预后相关。
晚期肝硬化的病程进展十分复杂,免疫因素在其中发挥了关键作用,即肝硬化相关性免疫功能障碍(CAID)[2]。CAID是一种免疫功能紊乱综合征,目前认为可能涉及免疫缺陷和全身性炎症反应两个方面。免疫功能紊乱与营养不良互为因果。营养不良以反复感染和慢性炎症为特征,促炎因子水平的升高常可以引起肝硬化患者食欲下降,进而使营养状况恶化。
中性粒细胞/淋巴细胞比率(NLR)是一个可靠的炎症指标,已被广泛用于评估各种病因所致肝纤维化/肝硬化的严重程度及预后[3]。本课题组已发表的研究结果表明,在出现急性肝功能恶化的肝硬化患者中,NLR的表达与血清IL-6/IL-8水平相关[4]。但目前尚无研究探讨NLR与RFH-NPT评估的营养不良风险之间的相关性。
基于上述问题,本课题组于2021年3月在JPEN J Parenter Enteral Nutr发表文章“Neutrophil-to-lymphocyte ratio is associated with malnutrition risk estimated by the Royal Free Hospital-Nutritional Prioritizing Tool in hospitalized cirrhosis”,旨在确定NLR的最佳截断值,以便更好地预测肝硬化患者营养不良的风险,并进一步阐明肝硬化患者NLR与营养不良之间的关系。
研究方法
该研究纳入135名住院的肝硬化患者,应用RFH-NPT对其营养状况进行筛查。首先评估患者有无急性酒精性肝炎或管饲的情况,其次区分伴有腹水或水肿的患者,最后计算相应得分。根据RFH-NPT评分,患者营养不良风险被划分为低(0分)、中(1分)和高(2~7分)三个等级。同时测量患者握力(HGS),将握力下降定义为:男性HGS<30 kg,女性HGS<15 kg。此外,本研究收集记录了研究对象的人口学信息、肝脏储备功能(MELD评分、CTP分级)、常见并发症(食管胃底静脉曲张、肝性脑病、腹水和感染)及临床生化指标,包括血清C反应蛋白(CRP)、NLR、血小板/淋巴细胞比率(PLR)、淋巴细胞/单核细胞比率(LMR)等用于评价免疫功能紊乱的指标。
研究结果
研究结果显示,通过ROC曲线分析,确定区分营养不良风险的最佳截断值为NLR>4.2(AUC=0.64,95%CI:0.55~0.74,P=0.004),其特异性为81.0%,敏感性为47.2%,阳性预测值为74.5%,阴性预测值为58.0%(图1)。相较于NLR≤4.2组,NLR>4.2组的患者更易出现营养不良高风险(74.5% vs 42.1%,P=0.002),且RFH-NPT评分显著高于前者(3 vs 1,P<0.001)。NLR>4.2组患者较NLR≤4.2组血钠水平及LMR更低,而MELD评分、PLR、CRP、血肌酐及酒精性肝病比例、合并腹水比例更高。此外,在营养不良高风险和握力下降患者中,NLR>4.2比例高于NLR≤4.2(图2,3)。
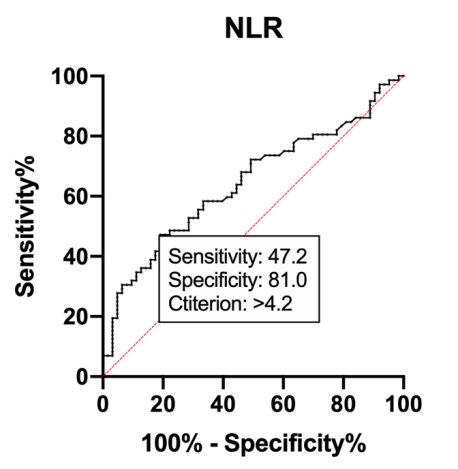
图1.ROC曲线及预测肝硬化患者营养不良高风险的NLR最佳截断值
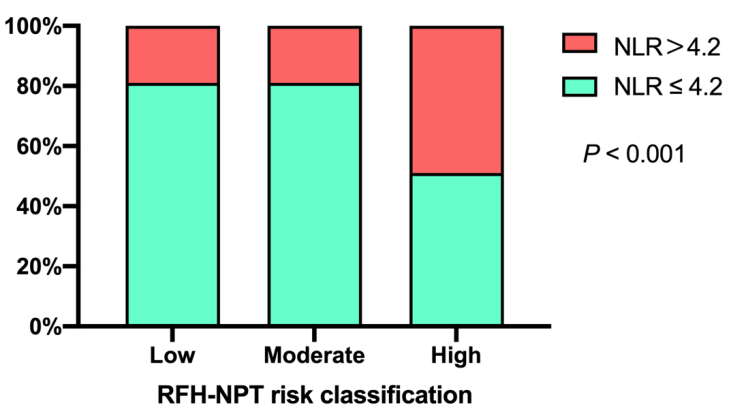
图2.按照RFH-NPT风险分组的肝硬化患者分布比例
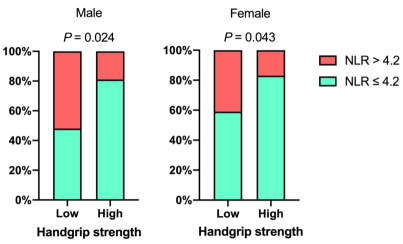
图3.按照男女握力分组的肝硬化患者分布比例
将肝硬化患者根据营养不良风险分为低/中危组和高危组,进行单因素logistic回归分析发现:男性、酒精性肝病、腹水、CTP-B/C级、腹围、NLR、白蛋白、肌酐和CRP是营养不良高风险的危险因素。进一步调整协变量后,NLR仍然是独立于酒精性肝病、腹水的营养不良的危险因素(OR=4.804,95%CI:1.395~16.547,P=0.013)。对NLR与HGS、RFH-NPT评分及肝功能指标进行相关性分析发现,NLR与HGS呈负相关(r=-0.22, P=0.031),而与CTP分级(r=0.22,P=0.010)、MELD评分(r=0.36,P<0.001)、RFH-NPT评分(r=0.31,P<0.001)呈正相关(图4)。
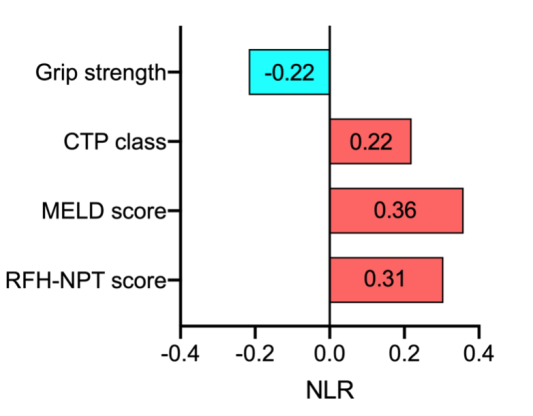
图4.NLR与肝脏储备能力、身体功能指标(握力)的相关系数
小结
肝硬化中免疫功能紊乱与营养不良的关系是复杂的,慢性免疫激活可能会增加营养消耗/需求,反复感染、肠道疾病和菌群失调又会进一步加剧该效应。及时评估和干预营养不良是肝硬化治疗中至关重要的部分,但至今尚未建立一致的营养筛查方法。根据既往的研究结果,课题组最终选定RFH-NPT对肝硬化患者进行营养状况分层。
本研究发现,在肝硬化患者中,应用RFH-NPT评估的营养不良高风险比例在NLR>4.2组和NLR≤4.2组中分别为74.5%和42.1%。腹水、酒精性肝病和NLR>4.2是营养不良高风险的独立预测因子。我们推测这可能由于腹水会机械性增加腹压导致患者摄食减少从而影响营养状况,而酒精性肝病患者本身罹患营养不良的比例就较高。
本研究还发现NLR与RFH-NPT以及HGS、CTP分级、MELD评分相关。事实上,HGS被视为全身肌肉力量的代表,且是营养状况和不良预后的独立预测因子。已有研究表明,营养不良的肝硬化患者肝功能更差且并发症发生率更高,因此NLR和慢性肝病评分系统(CTP分级,MELD评分)之间有很强的相关性就不足为奇了。
综上所述,用NLR衡量的免疫功能紊乱与用RFH-NPT评估的肝硬化患者营养不良风险相关。以CAID为靶点,可以为合并营养不良的肝硬化患者制定有效的治疗策略。
参考文献:(可上下滑动查看)
[1] Borhofen SM et al. The Royal Free Hospital-Nutritional Prioritizing Tool Is an Independent Predictor of Deterioration of Liver Function and Survival in Cirrhosis. Dig Dis Sci. 2016; 61(6):1735-43.
[2] Albillos A et al. Cirrhosis-associated immune dysfunction: distinctive features and clinical relevance. J Hepatol. 2014; 61(6):1385-96.
[3] Cai YJ, et al. A nomogram for predicting prognostic value of inflammatory response biomarkers in decompensated cirrhotic patients without acute-on-chronic liver failure. Aliment Pharmacol Ther. 2017; 45(11):1413-1426.
[4] Lin L et al. Prognostic nomogram incorporating neutrophil-to-lymphocyte ratio for early mortality in decompensated liver cirrhosis. Int Immunopharmacol. 2018; 56:58-64.
通讯作者
孙超,副主任医师,本科毕业于北京大学医学部,天津医科大学医学/理学博士,日本兵库医科大学特别研究员。2020年度天津医科大学总医院“十佳科技工作者”,天津市“131”创新型人才。全国疑难及重症肝病攻关协作组成员。主持完成国家自然科学基金一项。担任SCI期刊Journal of Clinical and Translational Hepatology编委。Mediators of Inflammation, Frontiers in Pharmacology客座编辑。2020年在EASL做口头发言。获得APDW的“Travel Grant”和EASL的“Full Bursary”奖励。以通讯作者在Clinical Nutrition、Liver International、Cell Death & Disease、JPEN J Parenter Enteral Nutr等杂志发表SCI文章32篇,累积影响因子110余分。目前研究方向为调节性细胞死亡在急慢性肝损伤中的作用机制,衰弱、体成分异常、营养不良和睡眠障碍在慢性肝病患者预后中的作用和治疗手段。
第一作者
王晓雨,天津医科大学总医院消化内科医师、讲师,毕业于天津医科大学,获医学博士学位。多次在国内外会议上做口头发言,并获得iGES的Young Investigator’s Award。以第一作者身份发表SCI论文3篇,最高影响因子6.36。目前研究方向为慢性肝病与营养不良、衰弱、肌肉减少症之间的关系。
(来源:《国际肝病》编辑部)