资料显示,本导基因成立于2018年,专注于体内基因编辑和体外转基因治疗疗法开发的创新企业。公司从成立之初便备受投资机构关注,获得多家机构投资,其为何受到资本追捧?核心技术是什么?领先产品有哪些竞争优势?
近日,具有原创性递送技术的全球领先基因疗法开发企业上海本导基因技术有限公司(下称本导基因)成功完成A轮6000万元融资,本次融资由华控基金独家领投,恩然创投、隆门资本、ETP基金、英诺天使基金等多家机构跟投,探针资本担任本次融资独家财务顾问。资金将用于多个产品临床前与临床开发、实验室与团队建设等诸多方面。企业此前分别于2019年6月获得赛赋医药战略投资,2020年3月获得凯旋创投pre-A轮数千万元投资。
基因治疗已成为第三大革命性疗法,但递送技术依然是最大瓶颈
针对无药可治或有药难治的遗传性、感染性和退行性等疾病,基因治疗具有“一针治愈”的特点,近年来已成为继化学药、抗体药物之后第三大革命性疗法。
历经2012年第三代基因编辑技术CRISPR首次出现,到2020年3月CRISPR进行首次在体的临床试验,再到2020年10月CRISPR获得诺贝尔化学奖等里程碑事件,基因编辑技术日渐趋于成熟,但递送技术一直是基因编辑治疗领域的最大障碍。诺贝尔奖得主Jennifer Doudna在2020年1月在《Nature》杂志撰文认为“
递送可能仍然是基因编辑体细胞治疗的最大瓶颈”(Delivery remains perhaps the biggest bottleneck to somatic-cell genome editing)。
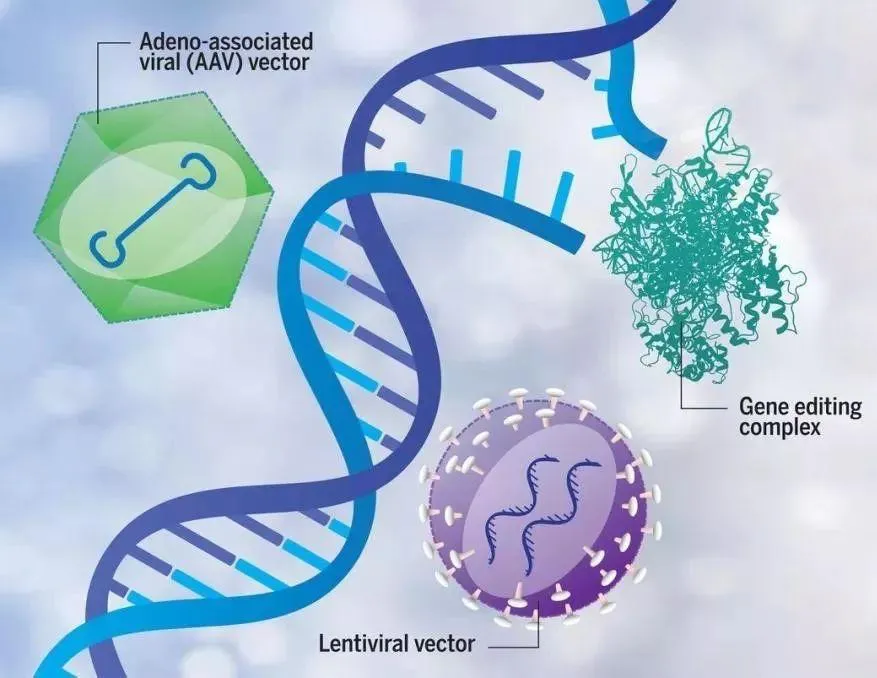
过去全球经过人体临床验证的基因治疗递送技术主要有腺相关病毒载体(AAV vector)、慢病毒载体(Lentiviral vector)、复合材料(Gene editing complex)三大平台。这些平台用于基因编辑递送均存在一定缺陷性。理想的基因编辑递送工具需要兼具瞬时和高效的特点,以确保治疗的安全性和有效性。
打造中国原创递送技术,助力基因治疗实现“从1到100”飞跃
本导基因创始人蔡宇伽博士先后师从瑞典卡洛琳斯卡医学院教授、诺贝尔奖委员会秘书长Thomas Perlmann教授和丹麦奥胡斯大学Jacob G. Mikkelsen教授,获得基因治疗专业博士学位。回国后,担任上海交通大学系统生物医学研究院研究员,掌握基因治疗载体的核心技术,具有丰富的基因治疗病毒载体工程化设计和改造经验。近年来公司成功开发经过人体临床验证的基因治疗递送平台——
VLP-mRNA(类病毒体mRNA),递送CRISPR/Cas9 mRNA以实现安全可控的体内基因编辑治疗。2020年11月初成功完成世界第二例在体CRISPR基因编辑治疗的临床研究(2020年3月,Editas公司张锋团队完成全球第一例),
也即全球第一例CRISPR抗病毒治疗的临床研究。该递送技术通过慢病毒外壳递送Cas9 mRNA,融合了
病毒载体感染细胞高效性(体外感染率99.8%、体内感染率>50%)和
mRNA表达瞬时性(72小时内降解)的优点,在不同疾病的动物模型上实现了治疗效果,具有在体内瞬时表达、无AAV表达CRISPR伴随的长期安全性风险、无明显脱靶、低免疫原性等技术优势。目前在复旦大学附属眼耳鼻喉科医院伦理委员会的论证及许可下,洪佳旭教授团队正在主持开展基于本项技术的初期安全可控的临床应用研究。
未来本项技术将拓展至其他病毒感染、眼科疾病和神经系统疾病的治疗。
华控基金董事长张扬先生表示,基因治疗行业具有市场空间巨大、技术门槛极高等特点,过去基因编辑技术实现突破、但递送技术依然是最大瓶颈,近年来本导基因创始人蔡宇伽博士及团队在基因编辑递送技术上成功实现了“从0到1”的创新突破。蔡宇伽博士过去10余年一直潜心开发基因治疗递送技术,先后成功开发出类病毒体CRISPR/Cas9 mRNA基因编辑递送技术、下一代慢病毒递送技术等多个原创性递送技术平台。公司原创性的病毒性角膜炎治疗产品,临床前动物实验数据极其完美,目前正在国内顶尖眼科医院进行非注册人体临床实验。企业同时布局了基因编辑技术治疗遗传性、感染性和退行性疾病、病毒载体治疗血液病、mRNA疫苗等多个产品管线。
谈到本次A轮融资由华控基金独家领投,张扬先生表示,非常感谢本导基因创始人蔡宇伽教授及老股东们的信任,未来将长期支持企业发展,共同推进本导基因的原创性递送技术和产品
实现“从1到100”的飞跃,使得未来有更多有药难治、无药可治的患者能够真正得到受益。
华控基金
华控基金成立于2007年,旗下拥有一系列投资于不同阶段和不同专业领域的VC、PE、产业基金、并购基金、海外基金等20余支子基金,管理规模过百亿,致力于成为中国最优秀的私募股权投资机构,专注于生物医药、高端制造等行业私募股权投资,长期坚持“价值投资”、“研究先行”的投资策略。“价值投资”指华控基金始终坚持培养自己发现“即将成为伟大企业或有机会成为伟大企业”的能力,选择投资高增长细分行业中龙头企业,并与这些企业一起成长。“研究先行”指通过自上而下的行业研究寻找优质投资标的,目前已完成50余个行业研究报告、扫描150余个细分行业、储备1000多个项目和积累200多个专家资源,积累了丰富的专家和项目资源。我们先后通过行业研究否定仿制药、生物类似药、低值耗材、特医食品、家用设备、第三方诊断、医疗信息化系统等门槛相对较低、竞争激烈的行业,选择了对具有市场空间大、行业门槛高等特点的新型抗体药物、医药外包服务、体外诊断、高值耗材等行业进行重点投资和布局。
近年来随着新冠疫情利好医疗行业投资、医疗新基建将新增大量医疗器械采购需求、中国人口老龄化驱动医疗需求长期持续增长、创新技术加速涌现使得更多优秀企业不断崛起、医疗政策改革红利加速创新医疗项目价值提升、商业模式变革利好创新性小公司具有更大发展空间、退出途径增加驱动医疗行业投资退出方式更灵活等利好因素驱动,使得中国医疗行业涌现出大量投资机会。华控基金抓住这些历史性机遇重点布局医疗行业,目前已投资10余家具有原创性技术平台、产品管线领先的优秀细分行业龙头企业,其中多个项目已经成功IPO或者申报境内外上市阶段,未来将会助力更多优秀医疗企业快速发展。
延伸阅读:
2021年1月11日,蔡宇伽及其团队在国际顶尖学术期刊Nature Biotechnology杂志上首次公开全球首创的类病毒体递送CRISPR/Cas9 mRNA技术,利用该技术治疗病毒性角膜炎,在小鼠模型中成功将潜藏在三叉神经节的HSV-1病毒库清除,实现了病毒性角膜炎基因治疗“从0到1”的创新突破。

该项研究成果得到了Nature Biotechnology审稿专家的高度肯定和认可:该工作的结果通过多种技术手段相互印证,罕见地表达出高度赞赏,数据质量近乎完美(the quality of the data is near exceptional),令人信服,该研究是对抗病毒领域的杰出贡献(make an excellent contribution to the field)。
同期,蔡宇伽团队在《Nature Biomedical Engineering》杂志上公布了CRISPR/Cas9 mRNA类病毒体递送基因编辑技术在湿性老年黄斑变性治疗上的临床前实验数据。

本导基因的CRISPR-Cas9 mRNA类病毒递送基因编辑技术同时也得到眼科顶级临床专家的高度认可:
(1)中山大学中山眼科中心副主任袁进教授:将基因编辑运用于单疱病毒性角膜炎的治疗无疑是 0 到 1 的创新突破。该研究证实在单疱病毒性角膜炎动物模型上通过基因编辑可抑制 HSV 病毒的转运和复制,有希望成为一种病毒性角膜炎的全新疗法,解决病毒性角膜炎复发这一临床难题。
(2)复旦大学附属眼耳鼻喉医院眼科副主任洪佳旭研究员:基因治疗行业一定是要选择一个好的医生资源来深度推进,蔡教授占据了华东地区最好的眼科资源。本次研究结果在人民日报等权威媒体上得到密集报道,同时各地政府和领导也非常重视,未来将有很多政策支持。
(3)中华医学会眼科分会角膜病学组组长、山东省眼科医院院长史伟云教授:长期以来,反复发作的病毒性角膜炎是临床治疗的难点。现有抗病毒与抗炎治疗并不能从根本上解决病毒潜伏于三叉神经元的问题。上海交通大学蔡宇伽教授和复旦大学洪佳旭主任在国际顶尖期刊 Nature Biotechnology 发表的原创型的基因编辑治疗技术为病毒性角膜炎的根治提供了新的解决思路,值得期待。



