免疫治疗遍地开花,为癌症患者带来了更多希望,但免疫治疗药物特殊的作用机制也为临床管理带来了更大的挑战。
免疫治疗相关的肺部不良事件较为罕见,但有可能会导致严重的后果。由于临床症状和影像学表现通常不具有特异性,与其他的肺部疾病相似,因此免疫治疗相关肺炎的患者可能无法得到及时的诊断和治疗。
由此,免疫治疗患者的影像学评估对于及时检出和正确管理免疫治疗相关肺炎具有重要意义。这一不良事件在影像学上可以呈现为肺炎样和结节病样表现,但临床中患者的表现往往变化多端,还会随着时间的推移而不断演变,患者本身的慢性阻塞性肺病、肿瘤进展、肺纤维化等疾病基础更让肺部不良事件的鉴别困难重重。

特稿发表在J Thorac Oncol杂志
因此,最近发表在J Thorac Oncol上的特稿就以9个经典的病例介绍了这一不良事件的8种可能的影像学表现,包括机化性肺炎(organizing pneumonia,OP)、非特异性间质性肺炎(nonspecific interstitial pneumonia,NSIP)、过敏性肺炎(hypersensitivity pneumonitis,HP)、急性间质性肺炎/弥漫性肺泡损伤(acute interstitial pneumonitis/diffuse alveolar damage,AIP/DAD)、细支气管炎(bronchiolitis)、肺结节或肿块样病变(pulmonary nodules or mass-like lesions)、结节病样表现(sarcoidosis like)以及无法分类的表现(unclassifiable pattern)。同时,特稿还为大家提供了这8种影像学表现的鉴别诊断思路。
▌ Case 1
男,65岁,伴骨、肺转移的肾细胞癌患者。患者自2016年9月起接受纳武利尤单抗治疗,2016年12月接受了椎体转移瘤放疗。因为呼吸困难接受了胸部CT检查,发现免疫治疗相关性肺炎(A、C);但胸片为阴性(B)。

Case 1 胸部CT、胸部X线平片、胸部CT
Learning Point:
接受过或正在接受免疫治疗的患者出现任何新的呼吸系统症状应该接受影像学检查,由于多达25%的患者胸片为阴性,因此应该首选高分辨率CT。
▌ Case 2
女,64岁,转移性黑色素瘤患者。患者在2017年6月至2017年9月接受了联合免疫治疗,随后接受了纳武利尤单抗维持治疗。患者曾在2017年9月被诊断为鼻病毒性细支气管炎(A);PET/CT再分期时偶然发现免疫治疗相关性肺炎(B),FDG摄取轻度增高,呈无法分类的表现;自由呼吸采集的CT图像由于呼吸伪影难以确定病灶特点(C);高分辨率CT证实了磨玻璃病灶(D)。
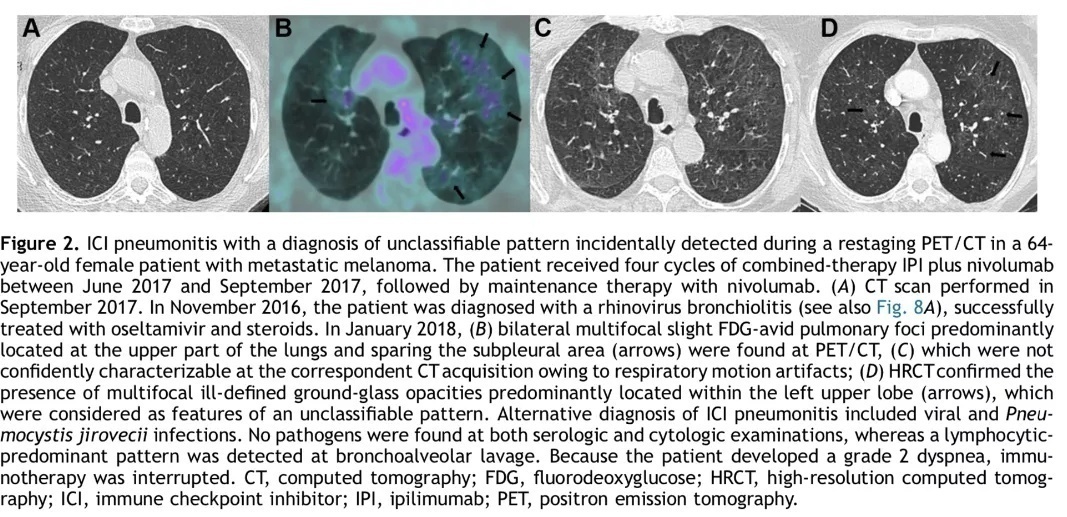
Case 2-1 胸部CT、胸部PET/CT、胸部CT、高分辨率CT
患者在鼻病毒性细支气管炎期间,胸部CT发现右肺上叶广泛的小叶中心型微结节,出现树芽征伴有支气管壁增厚和支气管扩张(A)。
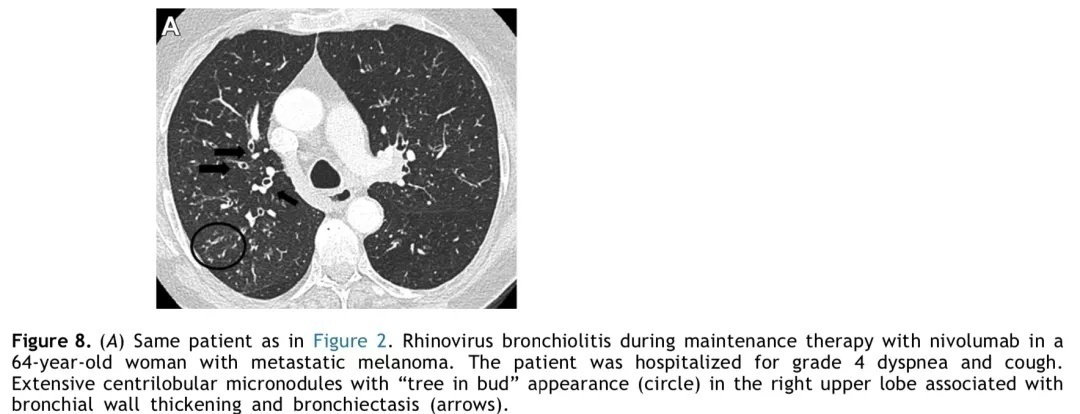
Case 2-2 胸部CT
Learning Point:
免疫治疗相关性肺炎和其他炎症一样FDG摄取增高,甚至可以在症状出现之前就检测到,但自后呼吸采集的CT图像由于呼吸伪影、切片厚度和视野较大等因素,也有可能出现磨玻璃结节,让免疫治疗相关性肺炎识别困难。
因此,如果新出现的病灶不太可能是转移时,可以在支气管肺泡灌洗检查之前,先做高分辨率CT以更好地评估病灶。
▌ Case 3
男,75岁,肝细胞癌患者,曾接受化疗栓塞和射频消融治疗。患者在2017年8月至2017年10月期间接受了4个周期的纳武利尤单抗治疗,但由于疾病进展而暂停。3个月后,患者出现呼吸困难、咳嗽、乏力和胸痛。CT发现胸膜下磨玻璃结节,支气管肺泡灌洗后发现以淋巴细胞为主,排除肺部感染(A);随后病灶演变为支气管血管周围和胸膜下条索样实变(B)。最终诊断为表现为机化性肺炎的免疫治疗相关性肺炎。

Case 3 胸部CT、胸部CT
Learning Point:
免疫治疗相关性肺炎最为常见的表现是机化性肺炎。
▌ Case 4
男,80岁,伴肺、肝转移的腮腺癌患者。2017年6月,患者在接受帕博利珠单抗治疗期间并发铜绿假单胞菌肺炎。胸部CT显示急性间质性肺炎/弥漫性肺泡损伤表现(A-C);在抗生素和激素治疗下初步恢复后,2017年7月患者因呼吸衰竭插管住院,胸部CT显示病灶表现变化并出现胸腔积液(D-F)。支气管肺泡灌洗细胞学显示中性粒细胞性炎症,未发现病原体。患者随后接受大剂量激素治疗,并中断了免疫治疗。
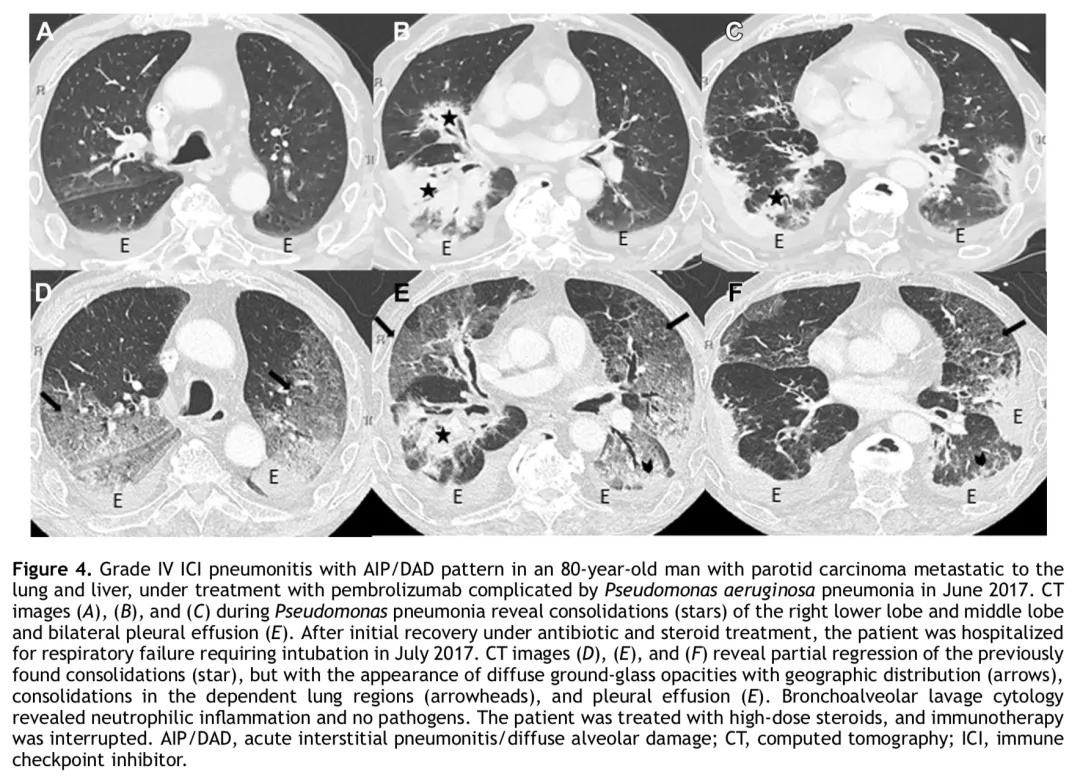
Case 4 均为胸部CT
Learning Point:
表现为急性间质性肺炎/弥漫性肺泡损伤的免疫治疗相关性肺炎很少见,但这一表现反映了疾病恶化,往往出现在临床情况最严重的病例之中。
▌ Case 5
男,63岁,伴肺、肾、肾上腺、骨转移的肺癌患者,其免疫治疗相关性肺炎呈结节样表现。患者在2015年7月至 2015年9月期间接受了联合免疫治疗,随后接受了武利尤单抗维持治疗。2016年1月胸部CT未发现结节(A);2016年4月胸部CT新发肺结节(B);2016年6月胸部CT结节增大(C),PET/CT检查提示轻度FDG摄取,提示恶性肿瘤(D)。患者接受了手术,但病理检查未发现肿瘤细胞,而是发现了慢性淋巴细胞炎症。之后,患者继续接受免疫治疗。
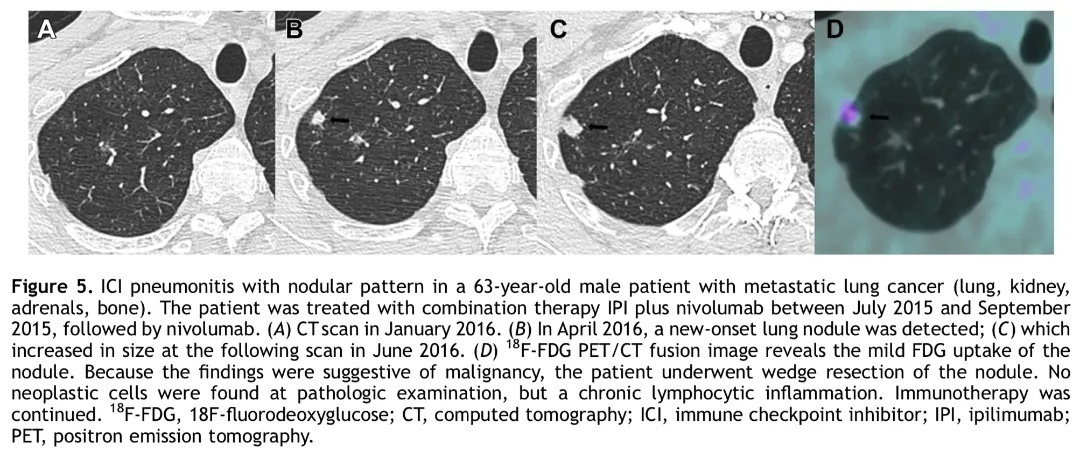
Case 5 胸部CT、PET/CT
Learning Point:
免疫治疗相关性肺炎可以表现为孤立的肺结节或肿块样病灶,有可能被误诊为恶性肿瘤。
▌ Case 6
女,50岁,转移性宫颈癌患者。患者免疫治疗前全身骨扫描发现全身多发FDG明显摄取病灶(A);免疫治疗后病灶均消失(B),提示疗效良好。然而,纵隔和肺门淋巴结出现了新的FDG摄取病灶(C),胸部CT发现叶间裂微结节(D)。患者接受了环磷酰胺治疗,随后的PET/CT检查发现纵隔和肺门淋巴结缩小,但出现了骨转移、上纵隔淋巴结转移和盆腔转移。
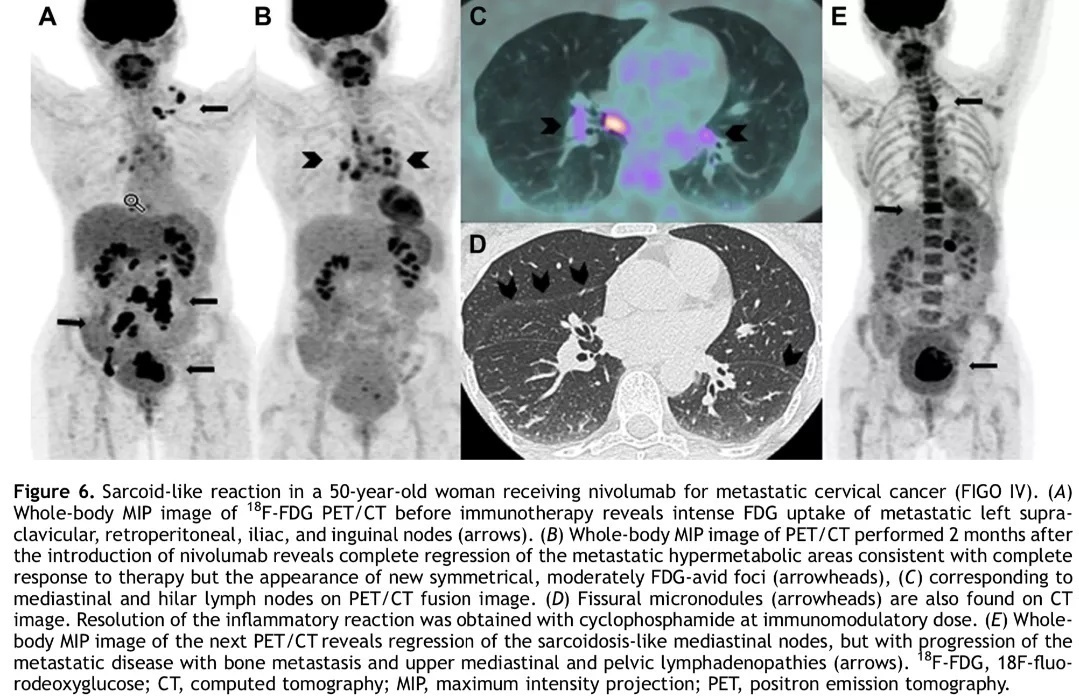
Case 6 全身骨扫描、PET/CT、胸部CT、全身骨扫描
Learning Point:
结节病样表现的免疫治疗相关性肺炎通常表现为对称性肺门和纵隔淋巴结肿大,常伴有两肺沿淋巴分布的微结节,包括支气管血管周围和叶间裂,病灶在PET/CT表现为FDG摄取。
▌ Case 7
男,59岁,伴脑、肺、小肠、骨、淋巴结转移的黑色素瘤患者。2014年6月,患者接受了右肺下叶转移灶切除术,随后接受了放疗。PET/CT检查中偶然发现之前放疗区域出现免疫治疗相关性肺炎(A-B)。2014年12月起,患者接受联合免疫治疗。2015年2月PET/CT检查再分期时发现放疗区域出现FDG摄取增高病灶(C),但患者并未出现相关症状;1个月后,患者因发热和呼吸困难入院,胸部CT发现右肺下叶病灶(D-E)。支气管肺泡灌洗检查以淋巴细胞为主,没有发现病原体或肿瘤细胞。患者中断了免疫治疗,接受了激素治疗。2015年8月,PET/CT检查显示肺部病灶吸收,残余实变符合纤维化表现(F)。在激素治疗期间,患者出现了肾上腺功能衰竭和机会性带状疱疹感染。
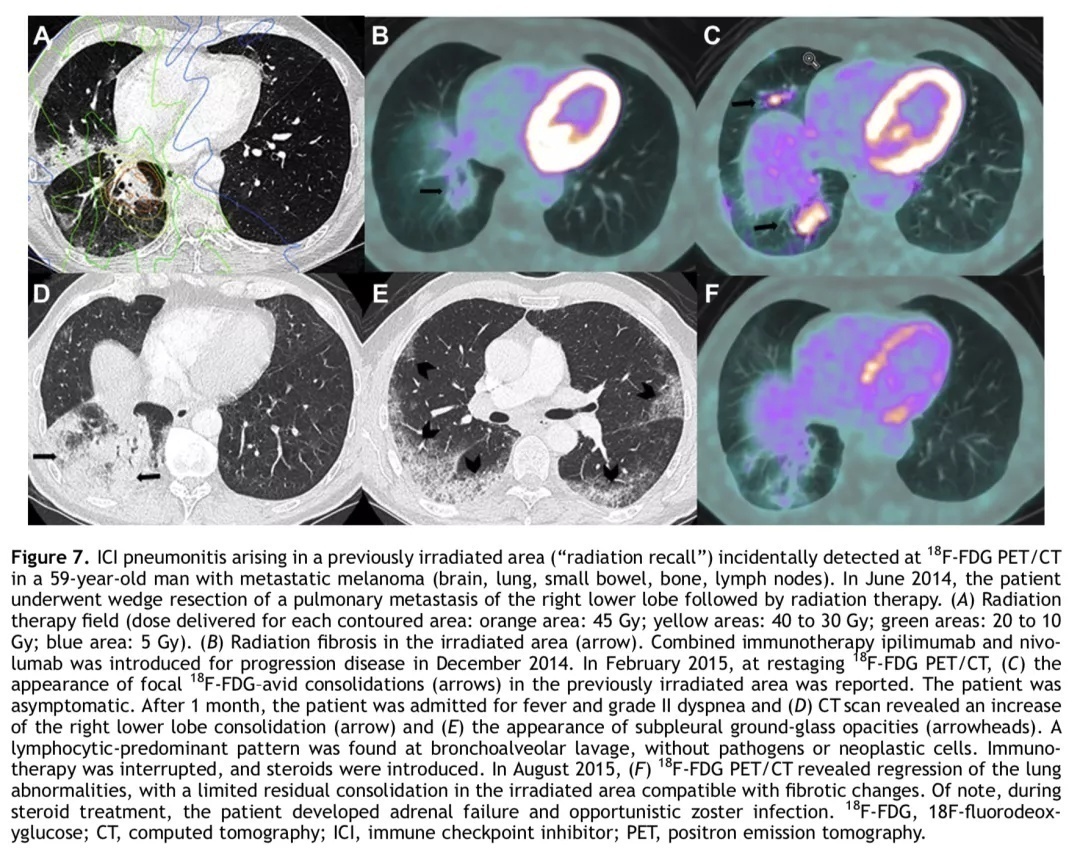
Case 7 放疗靶区、PET/CT、胸部CT、PET/CT
Learning Point:
肺部放疗之后可能会出现放射性肺炎,甚至数年之后也能昨日重现,出现所谓“放疗回忆”(radiation recall)现象。放疗区域的肺组织在免疫治疗的影响下可能会出现免疫治疗相关性肺炎,难以与感染或肿瘤复发鉴别。
虽然影像学特征有时能提示炎症,但通常患者都需要接受支气管肺泡灌洗检查。
▌ Case 8
女,44岁,转移性黑色素瘤患者,在联合免疫治疗期间出现军团菌肺炎。患者接受两个周期治疗后的PET/CT检查显示肺内出现摄取FDG的肿块(B),但患者没有相关症状。支气管肺泡灌洗证实了军团菌感染。
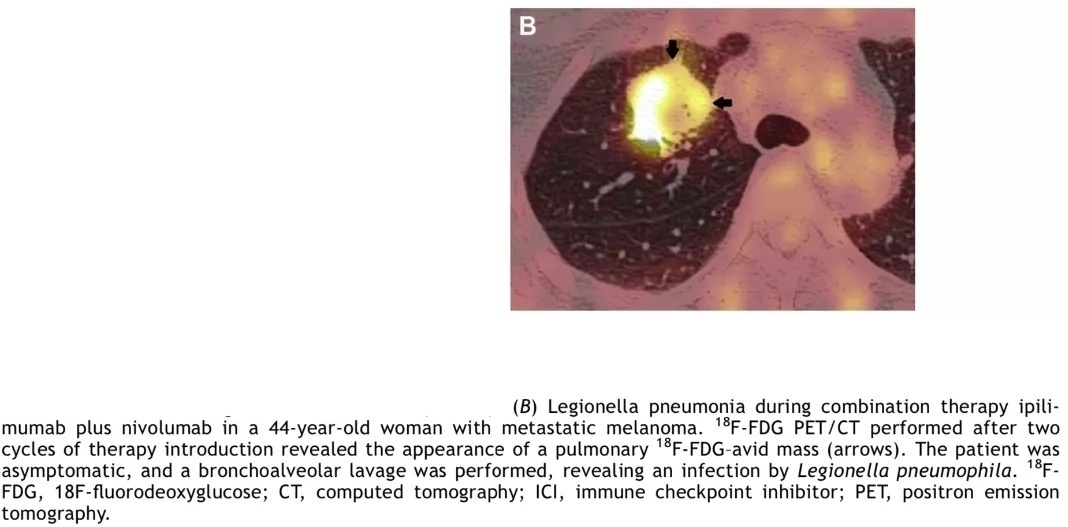
Case 8 PET/CT
Learning Point:
免疫治疗相关性肺炎的主要鉴别诊断包括感染和肿瘤进展,感染可以呈现为免疫治疗相关性肺炎的表现。
▌ Case 9
女,72岁,肺腺癌患者。患者于 2010年接受了右肺上、下叶切除术,随后接受了多线化疗。2013年7月,患者肿瘤进展,接受了姑息性免疫治疗。免疫治疗前胸部CT显示两肺肿瘤性病变(A);3月后复查病灶消失(B)。2014年6月胸部CT提示左肺下叶肿瘤复发,右肺下叶可能为其他性质病灶(C),但活检病理均为肿瘤。
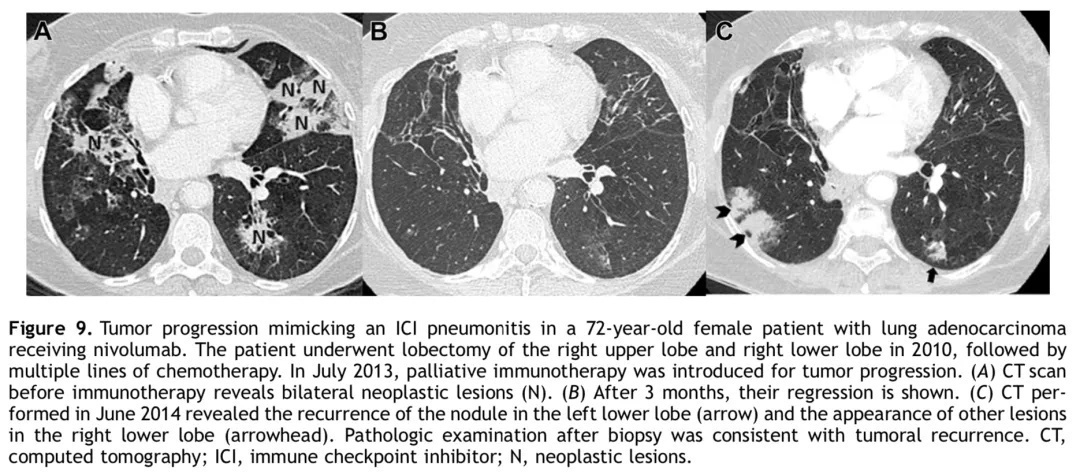
Case 9 均为胸部CT
Learning Point:
免疫治疗相关性肺炎的主要鉴别诊断包括感染和肿瘤进展,肿瘤进展可以呈现为免疫治疗相关性肺炎的表现。
▌ 总结
看完了这些实际的例子之后,特稿也不忘用表格的形式为大家画好了重点,总结了8种免疫治疗相关性肺炎的影像学表现和支气管肺泡灌洗检查的对应关系,由于免疫治疗相关性肺炎并没有明确的诊断标准,往往需要在排除了其他可能性之后才会给出这一诊断,因此特稿也为大家总结了8种影像学表现相应的鉴别诊断要点。
表 1 免疫治疗相关肺炎的影像-支气管肺泡灌洗检查结果对照
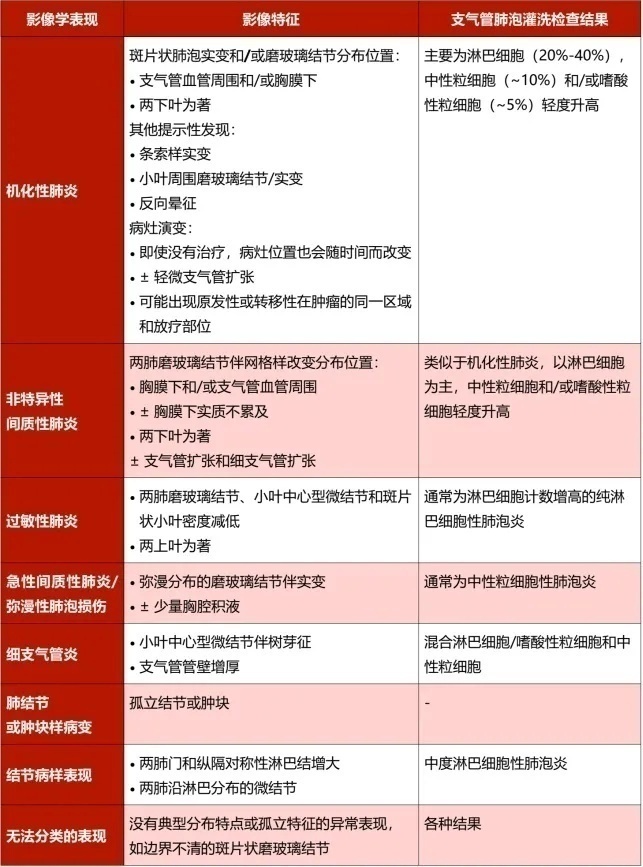
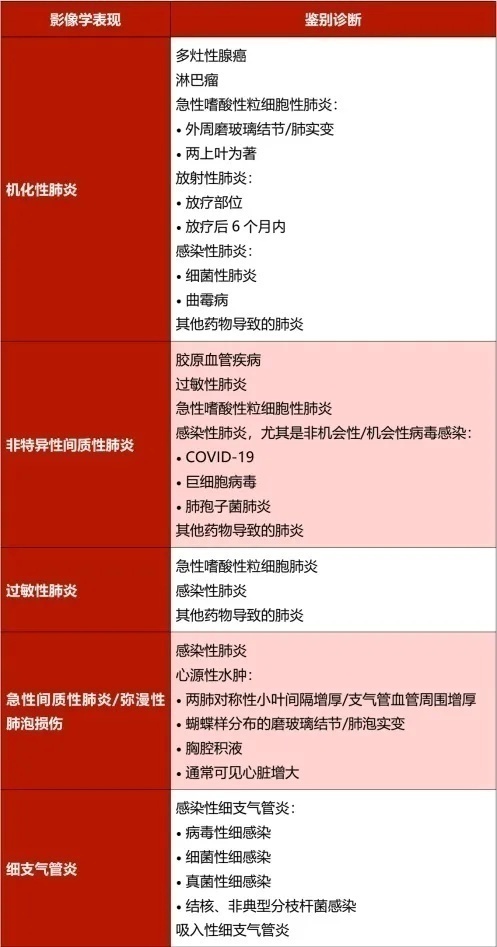
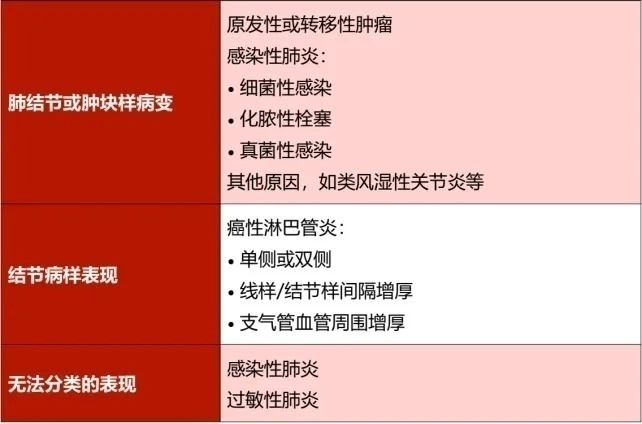
表 2 免疫治疗相关肺炎的影像鉴别诊断
患者的影像学表现并不能给出十二万分肯定的诊断,但对于无法接受其他支气管肺泡灌洗等侵入性检查的患者而言,影像学检查仍具有重要意义。
免疫治疗期间,免疫治疗相关肺炎虽然较为罕见,但仍有可能会导致临床危急情况。
因此影像科医师需要熟悉各种免疫治疗相关肺炎的影像学表现和鉴别诊断,以指导临床的诊疗。
参考文献:
[1] Pozzessere C, Lazor R, Jumeau R, Peters S, Prior JO, Beigelman-Aubry C. Imaging Features of Pulmonary Immune-related Adverse Events. J Thorac Oncol. 2021 Jun 1:S1556-0864(21)02188-2. doi: 10.1016/j.jtho.2021.05.017.