最值得注意的是,尽管以前所有的星形细胞肿瘤都被归为一类,但现在所有的弥漫性胶质瘤(无论是否为星形细胞)都被归为一类,不仅是基于它们的生长模式和行为,更重要的是基于它们共有的IDH1和IDH2基因状态。
从发病的角度来看,这提供了基于表型和基因型的动态分类;从预后的角度来看,它对具有相似预后标记的肿瘤进行分组;从最终治疗的角度来看,它可能会指导生物相似实体的治疗。
在这一新的分类中,弥漫性神经胶质瘤类别包括WHO II级和III级星形细胞肿瘤、II级和III级少突胶质细胞瘤、罕见的II级和III级少突胶质细胞瘤、IV级胶质母细胞瘤和相关的弥漫性神经胶质瘤(如儿童)。这种方法更清晰地将生长模式更局限、缺乏IDH基因改变、有时有BRAF突变(即毛细胞星形细胞瘤、多形性黄色星形细胞瘤和室管膜下巨细胞星形细胞瘤)的星形细胞瘤与弥漫性胶质瘤分开。换句话说,现在弥漫性星形细胞瘤和少突胶质细胞瘤在疾病分类学方面比弥漫性星形细胞瘤和毛细胞星形细胞瘤更相似;家谱已经重新绘制。类似地,尽管具有相似组织学表现的儿童和成人神经胶质瘤之间存在已知的行为差异,但儿童弥漫性神经胶质瘤以前与其整体(通常为成人)对应肿瘤归为一类。
关于儿童弥漫性胶质瘤独特的潜在遗传异常的最新信息促使这些实体从组织学相似的成人肿瘤中分离出来,其中一组肿瘤的特征是组蛋白H3基因K27M突变、弥漫性生长模式和中线位置:新定义的H3K27M突变弥漫性中线胶质瘤。在2016年WHO分类中使用综合表型和基因型参数提供了更高水平的客观性。这可能会产生比以前的分类更同质和更窄定义的诊断实体,这反过来会导致与预后和治疗反应更好的相关性。它还将导致潜在的更大的肿瘤组,这些肿瘤组不适合任何更狭窄定义的实体-这些组本身将更同质,因此更适合后续研究和改进的分类。
客观性提高的一个引人注目的例子与少突星形细胞瘤的诊断有关,少突星形细胞瘤是一种难以定义的肿瘤类别,在诊断中受观察者间高度可变性的影响,一些中心经常诊断这些病变,而其他中心很少诊断。
在诊断这些肿瘤时,基因型和表型的使用导致基本上所有的肿瘤都被归入与星形细胞瘤或少突胶质细胞瘤生物学相容的类别,只有少数病例同时具有这两种肿瘤的组织学和分子特征。
因此,星形细胞瘤和少突胶质细胞瘤更常见的诊断变得更加一致,少突胶质细胞瘤非常罕见的诊断也是如此。
上述对星形细胞瘤、少突胶质细胞瘤和少突星形细胞瘤进行分类的例子提出了一个问题,即分类是否可以仅基于基因型进行,即没有组织学。
在这个时间点,是不可能的;在分类过程中,必须首先在组织学上确定弥漫性神经胶质瘤(而不是其他肿瘤类型)的诊断,以便在适当的背景下理解特定遗传变化的疾病调查和临床意义。
表型仍然重要的另一个原因是,一些个体肿瘤不符合更狭义的基因型标准;例如,典型的弥漫性星形细胞瘤缺乏IDH1/IDH2和ATRX突变的特征性遗传特征。
然而,在更深和更广的基因组能力的背景下,未来世卫组织对弥漫性胶质瘤的分类可能需要更少的组织学评估——可能只是弥漫性胶质瘤的初步诊断。
目前,世卫组织目前的分类是基于表型和基因型联合分类的概念,以及所谓综合诊断的产生。
重要的是要认识到,改变分类以包括依赖于基因型的诊断类别可能会在检测和报告方面带来一定的挑战,这在其他地方已经讨论过。这些挑战包括基因分型和替代基因分型分析的可用性和选择,没有基因分型(或替代基因分型)能力的中心可能需要采取的方法,以及用于报告这些综合诊断的实际格式。
然而,在一些大型中心实施表型-基因型联合诊断,以及分子遗传改变的免疫组织化学替代物的可获得性越来越高,表明这些挑战在不久的将来很容易克服。
弥漫性星形细胞肿瘤的组织学分级
在神经肿瘤学中,组织学分级已被最系统地评估并成功地应用于弥漫性浸润性星形细胞肿瘤,尽管最近的研究表明,除了组织学分级提供的信息外,分子参数可能提供强有力的预后信息。然而,在世卫组织2016年的分类中,弥漫性星形细胞瘤采用类似于Ringertz系统、圣Anne-Mayo系统和世卫组织先前公布的方案的三层系统进行分级。
根据世卫组织目前的组织学定义,仅具有细胞学非典型性的肿瘤(如弥漫性星形细胞瘤))被视为 II级,那些还显示间变性和有丝分裂活性的肿瘤(如间变性星形细胞瘤)为WHO III级,另外显示微血管增殖和/或坏死的肿瘤为WHO IV级。
异型性被定义为伴随着深染的细胞核形状或大小的变异。核分裂象必须是明确的,但它们的数量或形态没有特殊意义。在大量样本中发现孤立的核分裂象并不足以证明 WHO III行为,但Ki-67增殖指数的测定可有助于区分II级肿瘤与III级肿瘤。
微血管增生被定义为内皮(而不是简单的高血管化)或肾小球血管的明显多层。
坏死可以是任何类型;坏死周围栅栏状不需要存在。
细胞区简单的并置,中间出现苍白色提示早期坏死是不够的。
上述标准使它们以可预测的顺序出现:非典型随后是核分裂象,然后是细胞增多,最后是微血管增生和/或坏死。
弥漫性星形细胞瘤,IDH突变型
【定义】
一种具有IDH1或IDH2基因突变的弥漫浸润的星形细胞瘤。
IDH突变型弥漫性星形细胞瘤的典型特征是中度多形性细胞,其特征是高度细胞分化和缓慢生长。存在ATRX和TP53突变支持该诊断。在缺乏1p/19q共缺失的情况下,形态学上类似少突胶质细胞瘤的成分的存在与该诊断相一致。这种肿瘤最常见于年轻人,发生在整个中枢神经系统,但好发于额叶。弥漫性星形细胞瘤具有恶性转化为IDH突变型间变性星形细胞瘤并最终发展为IDH突变型胶质母细胞瘤的内在能力。
【ICD-0编码】9400/3
【分级】弥漫性星形细胞瘤在组织学上对应于WHO II级。
【同义词】
低级别星形细胞瘤(不鼓励);
纤维型星形细胞瘤(不再推荐)
【流行病学】
①发生率
肿瘤登记处没有根据IDH突变状态区分弥漫性星形细胞瘤。然而,因为大多数病例携带IDH突变,可用的数据在某种程度上反映了这种基因定义的肿瘤实体。弥漫性星形细胞瘤约占所有星形细胞脑肿瘤的11~15%。每年的发病率估计为每10万人口中有0.55和0.75个新病例。一些报告表明,在一些北欧国家(斯堪的纳维亚国家)和北美,最近几十年儿童星形细胞瘤的发病率略有增加。男性多见,男女比例为1.3:1。
②年龄分布
IDH突变型弥漫性星形细胞瘤患者的中位和平均年龄约30岁。
根据一项仅针对成年患者的研究,IDH突变型弥漫性星形细胞瘤患者的中位年龄为36岁,平均年龄为38岁。这些价值与IDH突变型间变性星形细胞瘤相似。
【部位】
IDH突变型弥漫性星形细胞瘤可以位于中枢神经系统的任何区域,但最常见的发生在额叶的幕上。这类似于IDH突变和1p/19q共缺失的少突胶质细胞瘤的好发部位,并支持这些胶质细胞瘤是由不同的前体细胞群发展而来的假设。
【临床特征】
癫痫是一种常见的症状;然而,细微的异常,如言语困难,感觉或视觉的变化,以及某种形式的运动变化可能出现得更早。症状发作很少是突然的,有些肿瘤是偶然诊断的。
对于额叶肿瘤,行为或个性的改变可能是其表现特征。这种变化可能会在诊断前几个月出现。
【影像学】
像临床特征一样,神经影像学研究的结果可能极其多变。在CT上,弥漫性星形细胞瘤通常表现为低密度、界限不清、均质的肿块,无对比增强。然而,钙化和囊变可能出现在肿瘤发展的早期。核磁共振成像研究通常显示T1低密度和T2高密度,肿瘤发展早期区域增大。钆增强在低度弥漫性星形细胞瘤中并不常见,但往往在肿瘤进展过程中出现。
【肉眼检查】
由于其浸润性,这些肿瘤通常显示大体解剖边界模糊。侵入的解剖结构(如皮质和致密的有髓通路)有扩大和扭曲(但不是破坏)。局部肿块病变可能出现在灰质或白质中,但它们的边界模糊不清,可以看到较小或较大的囊肿、颗粒区域以及坚硬或软化区域等变化。囊性变最常见的表现是局灶海绵状区,有多个大小不等囊肿。大量微囊肿的形成可能会导致凝胶状外观。偶尔会出现一个充满透明液体的大囊肿。具有明显的肥胖细胞的肿瘤有时会有囊壁光滑的大单房囊肿。也可能出现局灶性钙化,可以观察到更弥散的沙砾。很少观察到延伸到对侧结构,尤其是额叶。
【显微镜检查】
弥漫性星形细胞瘤由分化良好的纤维型星形细胞组成,背景是结构松散,通常为微囊型肿瘤基质。
纤维型星形细胞瘤是典型的弥漫性星形细胞瘤,不再作为变异型。
与正常脑相比,细胞数量中度增加,核不典型是一个特征。通常无核分裂象,但是除非在小的活检或明显的核间变中观察到,否则单个核分裂象不能证明间变性星形细胞瘤的诊断是正确的。坏死或微血管增生的存在与弥漫性星形细胞瘤的诊断不相符。
从表型来看,肿瘤性星形胶质细胞的大小、细胞突起的突出和分布以及细胞质胶质细丝的丰富程度可能有很大差异。在肿瘤的不同区域,这种模式可能有明显的不同。
在切片上使用苏木精-伊红染色对肿瘤性星形胶质细胞进行组织学识别主要取决于核特征。
正常的星形胶质细胞核呈卵圆形至细长形,但在切片时,偶尔可见圆形横截面。典型的细胞核呈空泡状,有中等大小的染色质,通常有明显的核仁。正常的人星形胶质细胞没有显示出与背景神经细胞不同的可染细胞质。反应性星形胶质细胞由增大的细胞核和可染清晰的细胞质组成,最终形成肥胖星形细胞,该细胞具有丰富的嗜酸性细胞质,通常有偏心核,细胞质延伸到精细突起。
【鉴别诊断】
主要与反应性星形细胞增生进行鉴别。
因为大多数IDH突变型弥漫性星形细胞瘤有R132H突变,免疫组化检测R132H突变型IDH1(有时与p53标记物结合,很少与7三体结合)是区分肿瘤性星形细胞和反应性星形细胞的有力手段。然而,在其他情况下,鉴别诊断可能具有挑战性,可能依赖于标准的组织学差异。
弥漫性星形细胞瘤包含数量增加且通常大小增加的星形细胞,但很难在个体基础上与正常或反应性细胞区分开来。
在轻度间变中,星形胶质细胞的数量和(最常见的)其形态的一致性对识别其肿瘤性质最有帮助。反应性星形胶质细胞很少同时处于反应性的同一阶段,因此反应揭示了星形胶质细胞的混合物;一些细胞核增大,另一些细胞质数量不一,通常在稀薄的背景下。
在弥漫性星形细胞瘤中,几乎所有的细胞核看起来都是相同的,背景至少是正常密度或显示细胞突起数量增加。微囊性变可能存在,但大多数细胞看起来彼此相似,没有在损伤反应中更常见的肥胖细胞的混合。预先存在的细胞类型(例如神经元)常陷入其中。
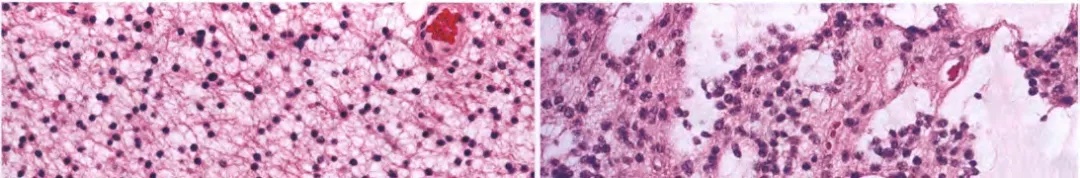
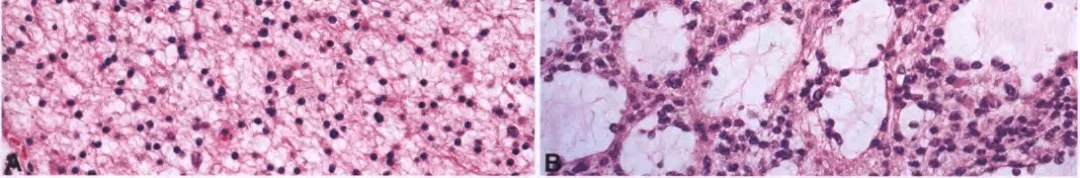
图1.弥漫性星形细胞瘤:一种中等细胞密度肿瘤,由一致的肿瘤性纤维星形细胞组成(左上和左下),可见广泛的微囊形成(右上和右下)
【生长分数】
由Ki-67增殖指数确定的生长分数通常小于4%。
与混合小细胞成分相比,肥胖肿瘤性星形细胞的增殖率明显较低。
然而,显微解剖显示,在肥胖细胞和非肥胖细胞肿瘤细胞中都有相同的TP53突变。
尽管已有报道称,肥胖细胞型可能特别容易发展为间变性星形细胞瘤和胶质母细胞瘤,但这并不能证明间变性星形细胞瘤的一般分类是正确的,这种印象也不是基于目前的分子特征,特别是对IDH突变状态的了解。
【免疫表型】
弥漫性星形细胞瘤可靠地表达GFAP,虽然程度不同且并不是所有的肿瘤细胞阳性。特别是,细胞质和突起稀少的小圆细胞,往往不表达GFAP。在这些病例中,免疫阳性可能局限于小的核周边缘和纤维性肿瘤背景中混合的肿瘤细胞。
波形蛋白也是典型的阳性表达,其标记模式与GFAP相似。
弥漫性星形细胞瘤的特征性分子特征(见遗传表达谱)通常可以通过免疫组织化学方法来证明。例如,R132H突变IDH1(IDH1 R132H突变约占所有胶质瘤相关IDH突变的90%)的表达可以使用突变特异性抗体来检测。
在突变肿瘤中,所有肿瘤细胞通常显示一定程度的细胞质(较强)和细胞核(较弱)标记,前提是所用的染色试剂是充足的。
因此,R132H突变IDH1免疫组织化学已成为一种非常重要的诊断辅助手段,不仅用于弥漫性胶质瘤的分子分层,还用于区分真正的肿瘤形成和反应性胶质增生。
还经常观察到细胞核强p53表达,这与弥漫性星形细胞瘤中TP53突变的高发生率一致。
然而,使用p53免疫组化阳性来反映TP53突变并不完全敏感或特异。
相比之下,ATRX的表达几乎总是在ATRX突变的情况下丢失,这在弥漫性星形细胞瘤中也是一突出特征(见遗传表达谱)。
ATRX通常在正常的、未突变的组织中表现出细胞核强阳性表达;因此,在非肿瘤性脉管系统和混合神经元、胶质细胞和小胶质细胞中ATRX阳性表达是准确解释ATRX阴性免疫染色模式的必要内对照。最后,与其不明显的核分裂象一致,弥漫性星形细胞瘤几乎总是具有小于4%的Ki-67增殖指数。
【细胞起源】
现有证据表明,IDH突变型和1p/19q共缺失少突胶质细胞瘤、IDH突变型弥漫性星形细胞瘤、IDH突变型间变性星形细胞瘤和IDH突变型胶质母细胞瘤是由不同于IDH野生型胶质母细胞瘤前体细胞的独特前体细胞群发展而来的。
【遗传表达谱】
世卫组织II级和III级弥漫性胶质瘤,包括弥漫性星形细胞瘤,几乎都以IDH基因突变为特征:IDH1或/DH2。发生在成人身上且不含IDH突变的弥漫性胶质瘤,无论其WHO等级如何,往往表现出更具侵袭性的临床行为。胶质瘤相关的IDH1和IDH2突变赋予各自的代谢酶IDH1和IDH2功能增加表型,这两种酶过量产生2-羟基戊二酸代谢物。具体来说,IDH突变诱导G-CIMP,通过这种方式,基因启动子区域的广泛高甲基化抑制了几种重要的细胞分化因子的表达。以这种方式,IDH突变和G-CIMP被认为将来源于神经胶质瘤的细胞保持在干细胞样的生理状态,这种生理状态本质上更易于自我更新和肿瘤发生。特别是,IDH突变似乎通过破坏染色体拓扑和允许诱导致癌基因表达的异常染色体调节相互作用来促进胶质瘤的形成,包括胶质瘤致癌基因如PDGFRA。与这一概念相一致,IDH突变似乎是弥漫性胶质瘤 WHO II级中发生的首批遗传改变之一。据报道,前IDH时代约50%的弥漫性星形细胞瘤存在MGMT启动子甲基化,但这一比例在IDH突变型弥漫性星形细胞瘤中可能更高,且与G-CIMP不一致。
绝大多数IDH突变型弥漫性星形细胞瘤,以及由其演变而来的WHO III级间变性星形细胞瘤和 IV级胶质母细胞瘤,也携带TP53和ATRX定义类别的功能缺失突变。ATRX编码一种必需的染色质结合蛋白,其缺乏与表观遗传失调和端粒功能障碍有关。特别是,ATRX突变似乎诱导了一种异常的端粒维持机制,称为端粒的交替延长。ATRX突变和端粒的交替延长与编码端粒酶催化成分的TERT基因的激活突变相互排斥。有趣的是,在绝大多数少突胶质细胞瘤和大多数IDH野生型胶质母细胞瘤中都发现了TERT突变。不同的端粒维持机制,由激活的端粒酶或端粒延长介导,似乎是所有弥漫性胶质瘤的发病机制所必需的。
ATRX缺乏也与普遍的基因组不稳定性有关,这在某些情况下会诱导p53依赖性细胞死亡。
因此,弥漫性星形细胞瘤中的TP53突变可能使肿瘤细胞在ATRX丢失的情况下存活。
IDH突变型弥漫性星形细胞瘤的基因组不稳定性反映在特征性的DNA拷贝数异常上,包括癌基因MYC和CCND2在互斥亚群中的低水平扩增事件。很少遇到通常与IDH野生型胶质母细胞瘤相关的拷贝数事件,如EGFR扩增和纯合CDKN2A缺失,这强调了IDH突变型和IDH野生型星形细胞瘤之间的生物学差异。在表达谱的基础上,根据IDH突变状态和神经胶质细胞谱系标记物分层,确定了多个弥漫性星形细胞瘤亚类。弥漫性星形细胞瘤的转录谱表明除了特定的基因组特征外,还有不同的细胞起源。