
在一项新的研究中,美国威斯康星大学麦迪逊分校细胞与再生生物学教授Beth Weaver领导的一个研究团队通过对患者样本的分析,发现了乳腺癌的一个关键特征使乳腺癌对紫杉醇治疗变得敏感或抗性,而且这可能被用来帮助识别哪些患者最有可能取得治疗成功。相关研究结果近期发表在Science Translational Medicine期刊上,论文标题为“Chromosomal instability sensitizes patient breast tumors to multipolar divisions induced by paclitaxel”。

Weaver说,“这是一个巨大的问题。近一半接受这种药物治疗的患者可能会出现一些相当大的副作用而没有任何治疗效果。”
这一发现的关键是在大约一半的乳腺癌中发现的由细胞不正常分裂时发生错误造成的染色体不稳定性。
身体中几乎所有的细胞都会分裂。这是有机体生长和适应的方式。在有丝分裂过程中,初始细胞的遗传物质以染色体的形式在两个相同的子细胞之间平均分配或“分离”。当它不能顺利进行时,染色体分布变得不平衡或“错误分离”,每个子细胞含有不正确数量的遗传物质。这是癌症的一种特征。
较低的错误分离率(染色体不稳定性)可以促使细胞开始不受控制地分裂,并导致肿瘤。然而,如果这种错误分离是极端的,它会导致细胞死亡。
这些作者发现表现出高水平染色体不稳定性的乳腺癌患者对紫杉醇更敏感,肿瘤抑制效果更好,这意味着它可能是紫杉醇治疗取得成功的难以捉摸的预测因素。
Weaver说,“这将具有巨大的意义。你可以在诊断活检留下的组织中测量染色体不稳定性,反正患者需要做这种活检,并有可能将这种组织用于生物标志物测试。”
Weaver从她读研究生时起就在实验室里研究紫杉醇,但她逐渐将重点转移到研究这种常用的化疗药物如何在乳腺癌患者的癌细胞中发挥作用。
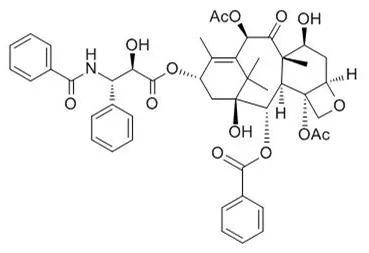
紫杉醇化学结构式
人们曾经认为,紫杉醇是通过阻止癌细胞分裂而发挥作用的。但在之前对使用标准、高剂量紫杉醇方案的患者进行的研究中,Weaver、她的同事Mark Burkard以及他们的研究团队发现这一模式并不成立。相反,他们发现该药物扩大了分裂中的癌细胞的错误分离。
Weaver说,“这向我们表明,我们在过去30年中认为紫杉醇的工作机制是错误的,这极其令人担忧。这使她和她的团队提出了这样的假设:紫杉醇可能通过引起或利用染色体不稳定性来发挥其抗癌作用。”
在这项新的研究中,这些作者能够研究不容易获得的乳腺癌样本,这些样本是在乳腺癌患者接受典型的低剂量紫杉醇方案治疗的生命周期的一个非常具体的时间点获得的。他们随后观察了细胞分裂过程中发生的情形。
在正常的细胞分裂过程中,细胞形成了称为纺锤体的结构,这些纺锤体附着在位于细胞中心的染色体上,然后像小绳索一样,在细胞开始分裂成两个子细胞时将遗传物质拉开。这有助于确保正确数量的染色体留在初始的细胞中,并被添加到新的子细胞中。
这些纺锤体被锚定在细胞两端或两极的一个位置上。然而,在接受紫杉醇治疗的患者的样本中,纺锤体在癌细胞中形成了多个极。这些癌细胞面临两种命运中的一种:异常的纺锤体在整个细胞分裂过程中保持不变;这些纺锤体最终“集中”返回到传统的双极纺锤体。当异常的多极纺锤体受到维持时,癌细胞死亡,肿瘤消退。当这些纺锤体集中返回到双极纺锤体时,癌细胞通常变得对紫杉醇更有抵抗力。
Weaver解释说,“了解这种集中返回是抗药性的主要机制,为首先确定新的药物靶点,然后开发使癌症对紫杉醇敏感的药物打开了大门。”
从整体上看,这些发现可能代表着癌症科学界对紫杉醇的理解向前迈出了一大步。Weaver说,即使许多非化疗疗法,如靶向疗法和免疫疗法,正在开发中以治疗乳腺癌,试图教这种老药一些新招数是有巨大好处的。
Weaver说,“我们真正想做的是把这种传统的化疗药物变成个性化的药物。这将是世界中最好的一种选择,因为紫杉醇被广泛使用,它很便宜,而且临床医生对它有大量的经验。如果我们能把它用于合适的病人,这将是癌症护理的一个巨大改进。”
参考资料:
Christina M. Scribano et al. Chromosomal instability sensitizes patient breast tumors to multipolar divisions induced by paclitaxel. Science Translational Medicine, 2021, doi:10.1126/scitranslmed.abd4811.