
原文:https://doi.org/10.1002/humu.24343
X 连锁肌营养不良症是最常见的肌营养不良症,在欧洲血统的新生男孩中的发病率为1:3800 至 1:6200,2010 年的患病率估计为每 10 000 名 5 至 24 岁男性中有 1.38 人患病。肌营养不良症包括杜氏肌营养不良症(DMD)、中度肌营养不良症(IMD)、贝克尔肌营养不良症(BMD)和极为罕见的X连锁扩张型心肌病;所有这些都是由编码肌营养不良蛋白的 DMD 基因突变引起的。DMD 是最严重的表型;这些男孩通常不表达抗肌萎缩蛋白,在皮质类固醇前时代,他们会在12 岁时失去行走能力,并在 20 岁或 30 岁时死于心力衰竭或呼吸衰竭。
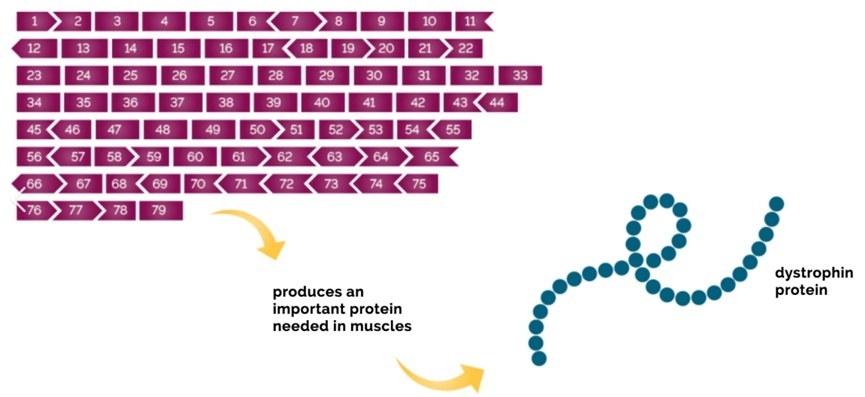
DMD 基因的长度接近 220万个碱基,有 79 个外显子,尽管 99% 的基因是内含子序列。一类未被充分认识的突变发生在基因的深内含子非编码区并导致内含子序列作为假外显子包含在内,普通临床中使用的基于基因组 DNA 的检测策略无法识别这些内含子变异,因为大多数使用拷贝数检测(通过 MLPA 等方法)与基因编码区测序的组合。标准临床突变分析方法(利用血液样本中的 DNA)对肌营养不良症患者的灵敏度在 93% 到 98.5% 之间。这表明剩余的肌营养不良症患者(高达 7%)将具有假外显子突变,这需要分析肌肉来源的 mRNA(通过 RT-PCR 生成的cDNA 测序或通过 RNA-Seq)进行鉴定。
在我们正在进行的大型研究队列中基因型/表型相关性的研究中,通过相关的临床突变分析,我们根据临床特征和肌肉活检中异常的肌营养不良蛋白表达对肌营养不良蛋白病患者进行了 mRNA 分析。因此,我们确定了 19 种导致这些患者 DMD 基因 RNA 改变的致病性深内含子变异或相关突变,进一步突出了肌营养不良症的基因型复杂性。
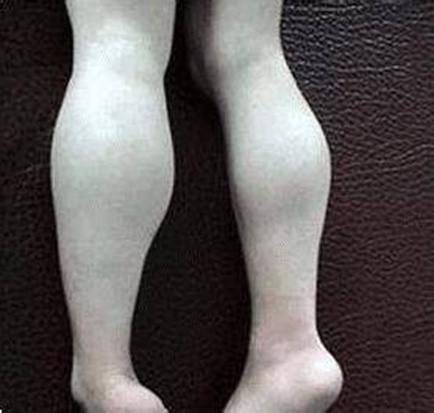
来自 UDP 的 1,344 名受试者中有 1,259 名临床测试的 DMD 突变呈阳性。在这些样本中,我们确定了 19 名具有临床特征、营养不良性肌肉活检和与肌营养不良蛋白病一致的肌营养不良蛋白表达的患者,这些患者具有深内含子或其他致病性变异,导致 DMD RNA 转录物改变。出于表 1 中概述方便,我们描述了三种一般类型的突变:1 型,由点突变组成;2型,由多核苷酸缺失或插入组成;和 3 型,由较大的染色体重排/易位组成。
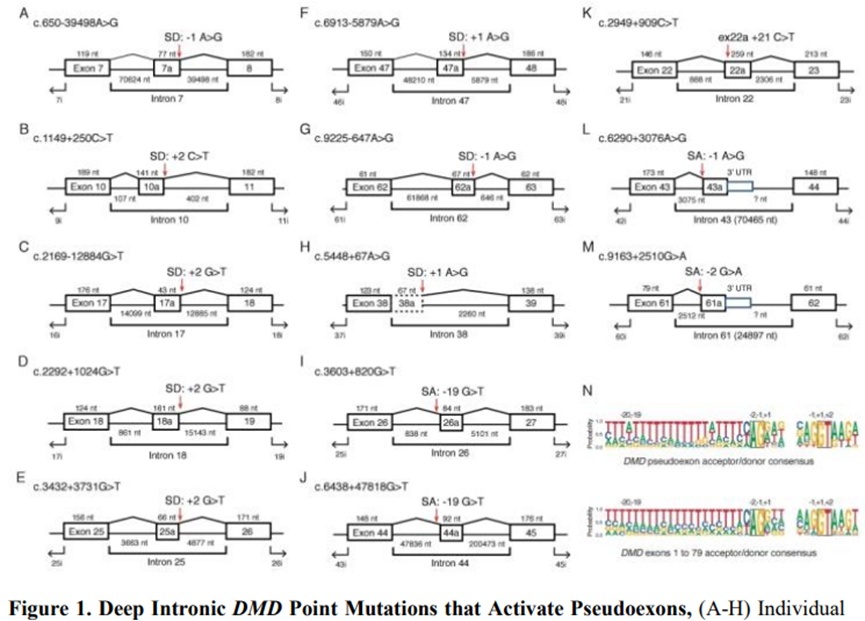
最大的一组由点突变(1 型)组成,这是一种产生假外显子的突变,之前已被鉴定和充分描述,在这个队列中,我们发现了八个 1a 型点突变,它们产生了剪接供体或受体位点(图 1A-H),两个 1a 型点突变去除了一个诱饵剪接受体位点(图 1I,J),一种 1b 型,它产生/破坏外显子剪接增强子/沉默子基序(图 1K),导致利用神秘的剪接供体和受体信号,以及一类新的两种 1c 型点突变,产生剪接受体位点(图 1L 和 M ) 导致形成伪 3'-末端外显子。
三名患者有 2 型突变(图 2A-C),包括多核苷酸缺失或插入
具有 3 型突变的患者代表更大规模的染色体重排,并且都具有 DMD 表型。一名患者通过 RT-PCR 分析检测到一个带注释的 chr2 lncRNA 外显子(来自 NR_131227.1 的外显子 2)(图 2D),表明该染色体 2 基因组区域的一部分已插入 DMD 内含子 55。RNA-Seq 分析解决了最后两种情况,即染色体 X OFD1 区域转座为 DMD 内含子 1(图 2E)和染色体 X 短臂倒位(图 2F)。
结论
本文提出了一种可通过肌肉 RNA 分析识别的三种不同类型突变的新分类,每种突变的潜在治疗方法都不同。识别和适当的表征可能会指导针对某些患者的全长肌营养不良蛋白表达的治疗。
对于DMD这类临床比较明确的遗传病,如果常规基因为阴性,非常值得使用二代或三代WGS科研分析,如果找到一个致病突变加上一些功能验证说不定就是一篇不错的文章。很多朋友也很疑惑WGS虽然检测到了内含子突变,但是内含子有那么多突变该如何筛选呢?游侠认为有三点可以考虑:一是只看目标基因的位点;二是只看罕见的变异;三是用spliceAI预测,这篇文章的附件中列出了spliceAI预测23个位点的结果,如果以0.2作为阈值的话,只有一个位点低于0.2,如下图。
