前言
2023年1月,为进一步科学、规范做好新型冠状病毒感染诊疗工作,《新型冠状病毒感染诊疗方案(试行第十版)》更新。在第十版的抗病毒治疗中,单克隆抗体安巴韦单抗/罗米司韦单抗注射液,小分子药物奈玛特韦片/利托那韦片、阿兹夫定片、莫诺拉韦胶囊,静注COVID-19人免疫球蛋白以及康复者恢复期血浆被列为推荐药物[1]。安巴韦单抗/罗米司韦单抗注射液(BRII-196/BRII-198)是我国首款获批的拥有自主知识产权的新冠中和抗体,用于治疗轻型和中型且伴有进展为重型(包括住院或死亡)高风险因素的成人和青少年(12-17岁,体重≥40kg)新型冠状病毒感染(COVID-19)患者,其中青少年适应症人群为附条件批准[2]。本文特邀武汉大学人民医院呼吸与危重症医学科的胡克教授分享三则新冠病毒感染临床案例,一同探讨新冠诊疗中抗病毒药物的治疗策略及中和抗体的应用场景和治疗特点。
中和抗体为免疫异常人群保驾护航
病例一
【基本信息】
一般情况:女性,68岁。
主诉:发热6天。
现病史:患者6天前无明显诱因出现发热,最高体温38.5℃,无昼夜规律,伴咳嗽、咳白黏痰。1天前出现胸闷,休息后可缓解,无咯血、头晕、头痛、恶心、呕吐、腹泻等不适症状。12月13日入院查胸部CT提示两肺炎性病变(图1),遂以“肺部感染”收入。
既往史:2019年10月因尿毒症行肾移植手术,术后口服免疫抑制剂:麦考酚钠肠溶片、他克莫司胶囊;有甲状腺病史,口服左甲状腺素钠片;10余年前行胆囊切除术。否认高血压、糖尿病、肝炎、结核病史。否认食物、药物过敏史。
体格检查:体温38.9℃,脉搏72次/分,呼吸21次/分,血压117/58mmHg,双肺呼吸音清,未闻及干湿性啰音。心脏、腹部查体未见明显异常。
【治疗经过】
入院实验室检查结果:新型冠状病毒核酸阳性,N基因Ct值20.99,ORF基因Ct值21.29。氧分压、SpO2正常;CRP 20.88mg/L(0~10mg/L,括号内为正常参考值范围,以下相同),PCT正常;肝功能正常,Cr 90μmol/L(41~81μmol/L),预估肾小球滤过率56.81mL/min(≥90mL/min);IgM 0.33g/L(8.6~17.4g/L),IgG 6.74g/L(8.6~17.4g/L)。诊断为中型新型冠状病毒感染。
入院当天(出现症状约1周)予以鼻导管吸氧、阿兹夫定片抗病毒、头孢哌酮3g q8h静滴、莫西沙星0.4g qd静滴抗感染、甲强龙40mg qd静滴抗炎、低分子肝素抗凝治疗后,患者胸闷稍解,但体温仍控制不佳。
2022年12月15日(入院第3天)复查胸部CT:两肺多发磨玻璃影、片絮状密度增高影,提示双肺感染较前(2022-12-13)进展(图2)。2022年12月16日实验室检查:氧分压109mmHg(83~108mmHg),SpO2、乳酸正常;WBC 2.42×109个/L(3.5~9.5×109个/L),中性粒细胞计数1.42×109个/L(1.8~6.3×109个/L),淋巴细胞计数0.73×109个/L(1.1~3.2×109个/L),CRP 23.58mg/L(0~10mg/L)。由于患者为肾移植术后,长期服用免疫抑制剂,请器官移植科会诊后暂停免疫抑制剂。治疗方案上加用丙种球蛋白10g增强机体免疫功能、米卡芬净抗真菌治疗。
2022年12月17日(入院第5天)再次复查胸部CT提示双肺感染病灶较前(2022-12-15)增加(图3)。12月20日患者诉喘气加重,伴间断咳嗽。实验室检查:SpO2 89%(鼻导管吸氧,氧流量5L/min)。淋巴细胞计数0.43×109个/L(1.1~3.2×109个/L),CRP 54.76mg/L(0~10mg/L),已进展为重型。治疗方案上停用莫西沙星,改为利奈唑胺抗感染,加用无创呼吸机辅助通气、雾化吸入化痰止咳治疗,余治疗不变。
2022年12月23日(入院第11天)患者仍有活动后气喘,精神较差,病情危重,加用1000mg/1000mg安巴韦单抗/罗米司韦单抗、胸腺法新治疗。2022年12月27日复查胸部CT提示双肺感染性病变较前(2022-12-17)好转(图4)。实验室检查:WBC、中性粒细胞计数正常,淋巴细胞计数0.42×109个/L(1.1~3.2×109个/L),CRP<3mg/L(0~10mg/L)回到正常值。
2023年1月1日(入院第20天)复查胸部CT提示双肺感染性病变较前(2022-12-27)进一步吸收(图5)。实验室检查:WBC、中性粒细胞计数正常,淋巴细胞计数0.58×109个/L(1.1~3.2×109个/L),CRP<3mg/L(0~10mg/L),患者肺炎症状好转。肾功能不全转器官移植科进一步治疗。
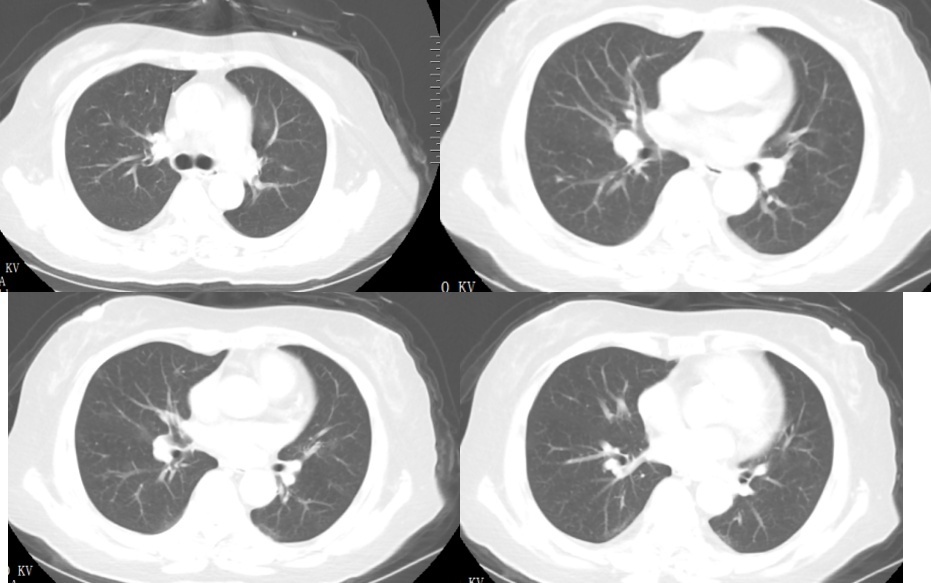
图1 胸部CT 2022-12-13(入院第1天)
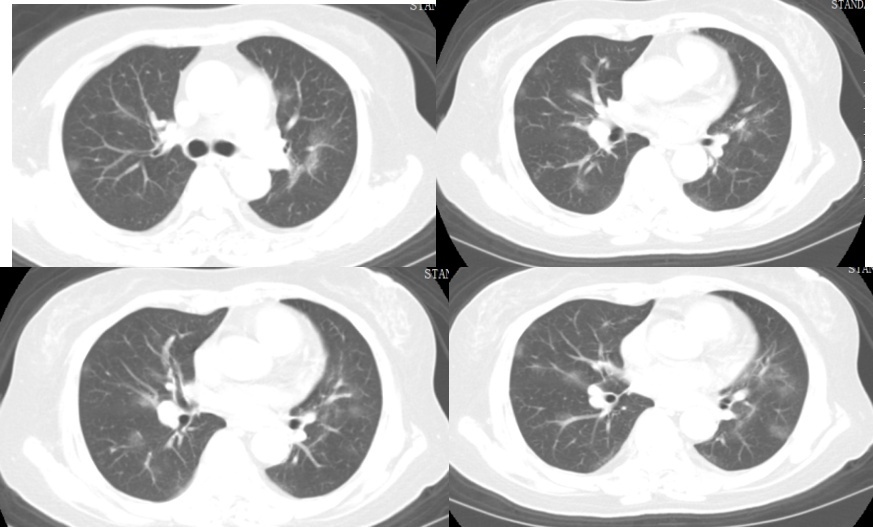
图2 胸部CT 2022-12-15(入院第3天)
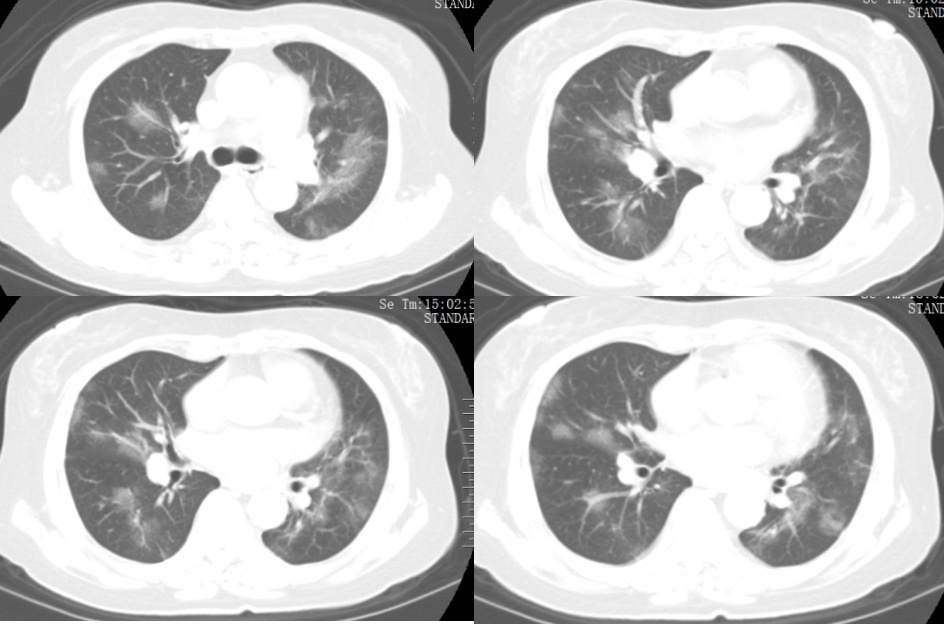
图3 胸部CT 2022-12-17(入院第5天)

图4 胸部CT 2022-12-27(入院第15天)
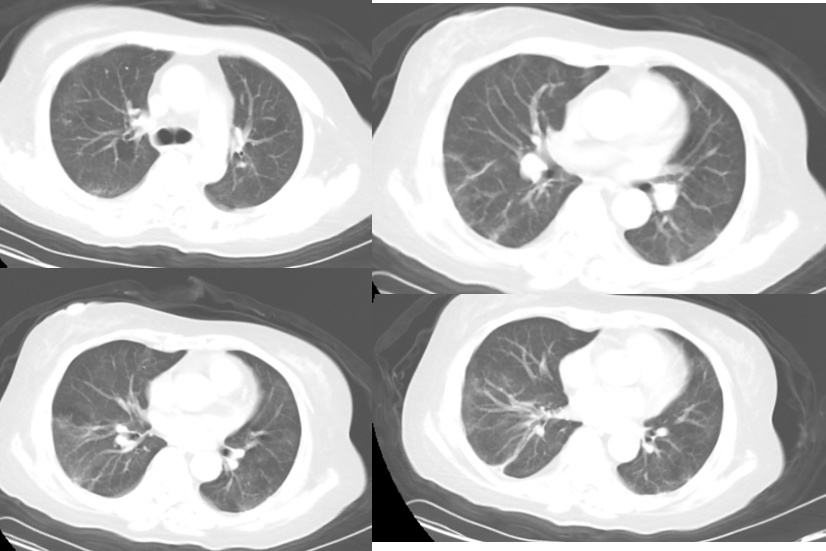
图5 胸部CT 2023-01-01(入院第20天)
病例二
【基本信息】
一般情况:女性,60岁。
主诉:间断发热3周。
现病史:患者3周前无明显诱因出现间断发热,最高体温39.2℃,伴畏寒、肌肉关节酸痛,偶伴头痛,咳嗽、咳少许白痰,有纳差、乏力,否认恶心、呕吐、胸痛、呼吸困难、咯血、腹痛、腹泻等不适。起病后1周至入院前曾于其他医院就医治疗(方案不详),未见明显好转,几次胸部CT检查提示疾病进展(图6、图7),为求进一步诊治于1月4日入院,门诊以“肺部感染”收入。
既往史:2019年因卵巢癌行卵巢子宫及双附件等切除术,术后辅以化疗6次,2021年因卵巢癌复发再行手术治疗(部分肠管切除),予以直肠造瘘,术后辅以化疗7次加免疫治疗1次,现口服靶向药物奥拉帕利2片bid,否认高血压、糖尿病、肝炎结核病史,否认输血史,否认药物食物过敏史。
体格检查:体温38℃,脉搏103次/分,呼吸20次/分,血压103/54mmHg,双肺呼吸音清,未闻及干湿性啰音。心脏、腹部查体未见明显异常。
【治疗经过】
入院后实验室检查:新型冠状病毒核酸检测阳性,N基因Ct值24.62,ORF基因Ct值25.23。氧分压77mmHg(83~108mmHg),SpO2正常;肝肾功能大致正常。诊断为中型新型冠状病毒感染。
入院当天予以鼻导管吸氧、雾化吸入化痰止咳、1000mg/1000mg安巴韦单抗/罗米司韦单抗抗病毒、莫西沙星0.4g qd静滴抗感染、甲强龙40mg qd静滴抗炎、低分子肝素抗凝等治疗。
2023年1月8日(入院第5天)复查胸部CT提示双肺感染较前(2023-1-3)好转(图8)。

图6 胸部CT 2022-12-26

图7 胸部CT 2023-1-3(入院前1天)

图8 胸部CT 2023-1-8(入院第5天)
在上述两则病例中,患者分别有器官移植/活动性肿瘤病史,且正在服用抗排异或抗肿瘤药物,属于临床上常见的免疫功能低下暨脆弱人群。这部分患者自身往往无法针对病毒感染产生有效的免疫应答(例如第一例肾移植患者因长期服用免疫抑制剂,感染新冠病毒后IgM、IgG均低于正常值),所以病毒的复制期可能延长[3-4],从而治疗也更加棘手。从核酸检测中也可以看到,两位患者的N基因和ORF基因的Ct值在感染超过1周时,仍低于28[5],提示病毒可能仍在复制。在这种情况下,虽然应用抗病毒治疗(如新冠中和抗体)已是发病后较长时间,但患者仍具有临床获益的病理生理基础。
适用场景探讨,重型患者亦可获益
病例三
【基本信息】
一般情况:男性,70岁。
主诉:咳嗽、咳痰、咽痛一周伴发热4天。
现病史:患者一周前无明显诱因出现咳嗽、咳黄白痰,伴有胸闷、气喘。4天前出现发热,最高体温38.9℃,伴有畏寒、肌肉关节酸痛,否认恶心、呕吐、胸痛、心慌、腹痛、腹泻等不适症状。发病以后自行予以对乙酰氨基酚、左氧氟沙星及阿兹夫定片口服治疗,未见明显好转,家属发现患者指脉氧低,为求进一步诊治于12月23日入院。
既往史:高血压病史5年,口服非洛地平缓释片5mg qd;有慢性胃炎、过敏性鼻炎病史;结肠癌术后12年。否认肝炎、结核病史。
体格检查:体温37.9℃,脉搏104次/分,呼吸20次/分,血压152/78mmHg,双肺呼吸音粗,未闻及干湿性啰音。心脏、腹部查体未见明显异常。
【治疗经过】
入院后实验室检查:新型冠状病毒核酸检测阳性,N基因Ct值22.11,ORF基因Ct值23.12。氧分压64mmHg(83~108mmHg),氧饱和度93%(95~98%);WBC、中性粒细胞计数正常,淋巴细胞计数0.43×109个/L(1.1~3.2×109个/L),CRP 133.33mg/L(0~10mg/L);ALT 77U/L(9~50U/L),AST 109U/L(15~40U/L),Cr 135μmol/L(57~111μmol/),预估肾小球滤过率79.88mL/min(≥90mL/min);IgM 1.78g/L(0.3~2.2g/L),IgG 7.68g/L(8.6~17.4g/L)。胸部CT提示:双肺多发斑片状、磨玻璃、片絮状密度增高影(图9)。诊断为重型新型冠状病毒感染。
入院后当天予以无创呼吸机辅助呼吸,雾化吸入化痰止咳,1000mg/1000mg安巴韦单抗/罗米司韦单抗、阿兹夫定片抗病毒,头孢哌酮3g q8h静滴、莫西沙星0.4g qd静滴抗感染、甲强龙40mg qd静滴抗炎,丙种球蛋白10g增强机体免疫功能,低分子肝素抗凝等治疗。
2022年12月27日(入院第5天)复查胸部CT提示双肺多发片状玻璃影,较前(2022-12-23)好转(图10)。CRP 10.59mg/L(0~10mg/L),ALT 122U/L(9~50U/L),AST 69U/L(15~40U/L),Cr 80μmol/L(57~111μmol/L),预估肾小球滤过率85.95mL/min(≥90mL/min)。
2023年1月9日(入院第18天)复查胸部CT提示双肺感染较前(2022-12-27)进一步吸收、减轻(图11),复查新冠病毒核酸阴性。
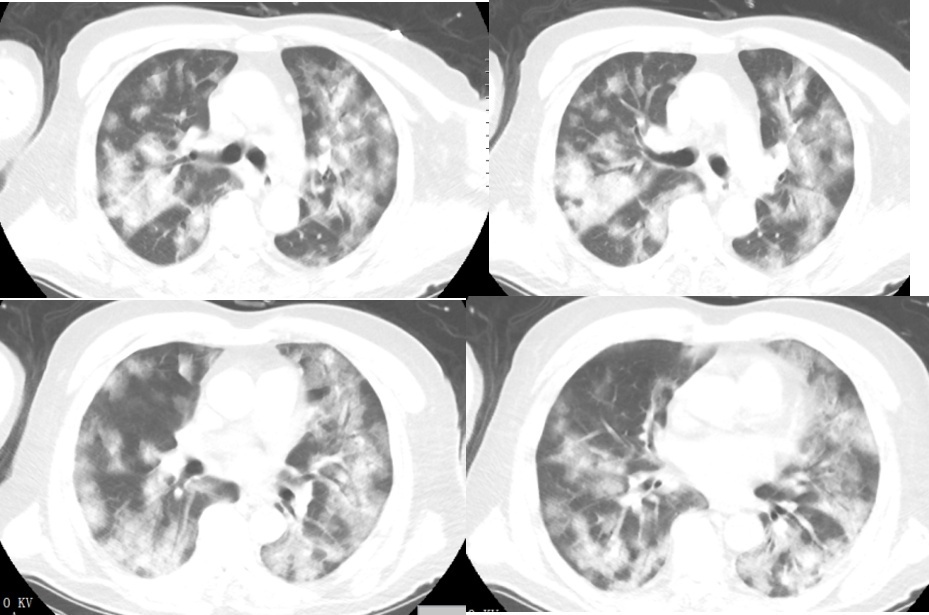
图9 胸部CT 2022-12-23(入院第1天)
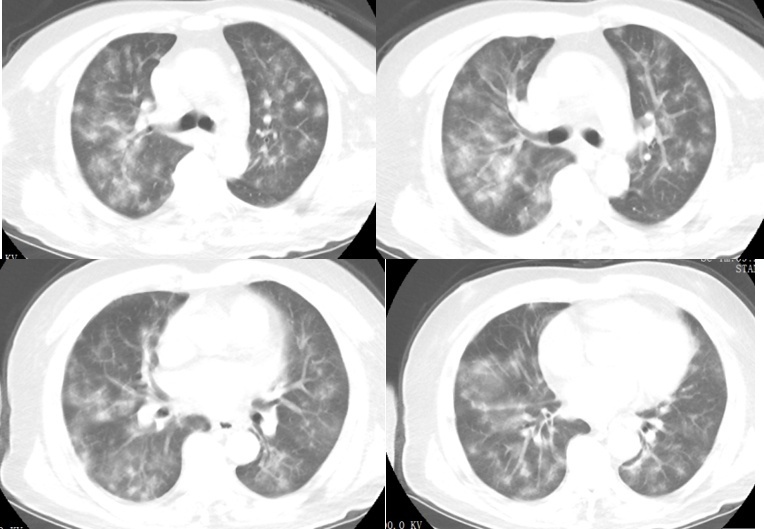
图10 胸部CT 2022-12-27(入院第5天)
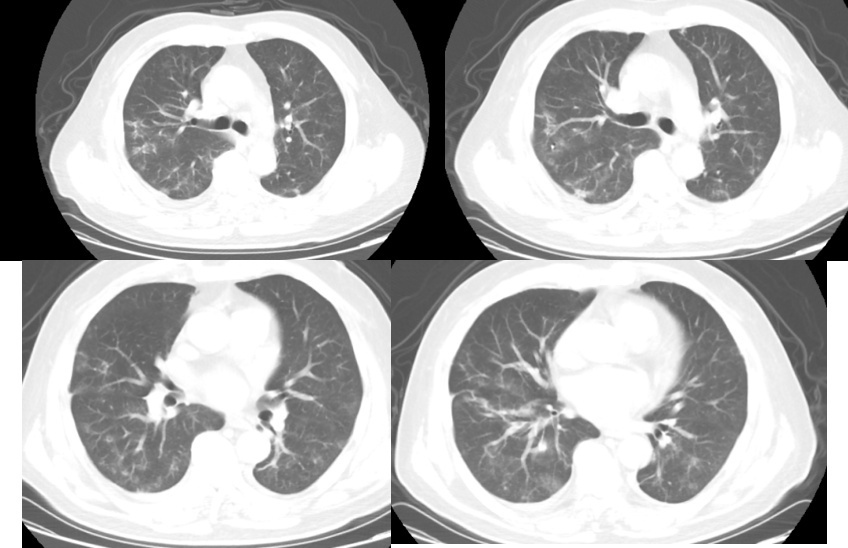
图11 胸部CT 2023-1-9(入院第18天)
本案例为高龄伴慢性基础疾病(高血压)的新冠病毒感染患者,入院时虽然已符合重型标准,但仍处于发病后较早期(症状出现约1周),此时核酸检测Ct值偏低,提示病毒仍处于复制期,存在抗病毒药物应用的理论基础。因此及时采用抗病毒药物(如新冠中和抗体)配合其他治疗手段,用药后改善较为明显。这提示即使是重型患者,只要仍存在病毒复制的证据且发病时间较短,患者仍可能从抗病毒治疗中获益,而且也提示早期抗病毒治疗的重要性。
新冠中和抗体机制及特点剖析
持续守护脆弱人群
在本篇分享的三则病例中,患者有器官移植并服用免疫抑制剂、活动性肿瘤病史、高龄伴基础病等风险因素,属于在疾病防护和治疗中需要重点关注的脆弱人群。在临床工作中,患者的实际情况往往错综复杂,应用抗病毒治疗时有可能出现超时间窗、超适应症等情况,需要医生根据病情进行判断和个体化治疗。如本文提到的脆弱人群,因为自身的免疫状态较差,病毒的复制期可能延长[3-4],此种状态下及时、准确进行抗病毒治疗(如中和抗体)可能使患者临床获益。因此对某些患者,临床上可以采用IgM和IgG辅助判断患者的免疫状态(有条件的医院采用SARS-CoV-2特异性IgM和IgG更佳),采用核酸检测Ct值来辅助判断病毒的复制情况,进而为患者采取相应的治疗措施。
在作用机制上,安巴韦单抗可以阻断病毒与宿主细胞ACE2受体的结合,罗米司韦单抗可以抑制病毒与细胞膜融合必须的S蛋白重排,从而阻止病毒进入细胞,双抗体联合可以更好地减少免疫逃逸,使疗效更加强效稳定。同时,中和抗体还可通过下游免疫机制清除病毒及被感染细胞,减轻炎症反应[6],使几乎不能产生抗体或产生抗体水平较低的脆弱人群从中获益。
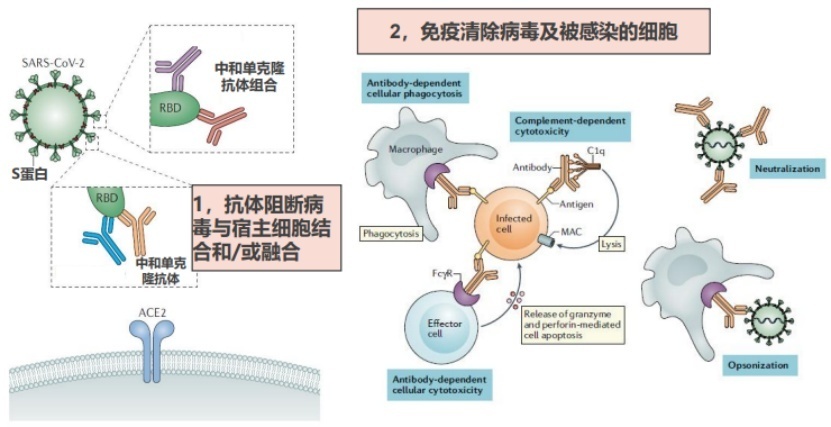
图12 新冠中和抗体多机制示意图[6]
安巴韦单抗/罗米司韦单抗能够显著降低患者的重症和死亡风险80%[7],体外中和试验证实对目前国内正在流行的主要变异株(如奥密克戎BA.4/5、BF.7等)保持抗病毒活性[8-9]。在临床应用时,单次静脉输注即可获得高效抗体,无需考虑药物-药物相互作用,无需根据肝肾功能调整用药,治疗时间窗也更长(发病10天以内,相较于小分子药物如Paxlovid的5天以内[10]),这使得中和抗体的使用更加安全便捷。Ⅰ期研究显示,安巴韦单抗/罗米司韦单抗的半衰期分别为44.6-48.6天/72.2-83.0天[11],远长于小分子药物如Paxlovid的6小时[10]。对于正常人群来说,患者在新冠病毒感染后7天,SARS-CoV-2特异性IgM和IgG血清阳性率就可超过70%[12],但免疫状态较差的患者产生相应抗体则需要更长的时间,在这种情况下,可长时间维持疗效的中和抗体可能给患者带来更多获益。
中国疾病预防控制中心报告显示,目前我国主要流行变异株为BA.5.2和BF.7系列[13],同时根据2023年1月湖北省疾病预防控制中心的监测数据,湖北省流行的奥密克戎变异毒株以BA.5.2为主[14]。本文的分享病例提示了安巴韦单抗/罗米司韦单抗对目前中国主流毒株的临床有效性,且相关研究也表明,安巴韦单抗/罗米司韦单抗联合疗法对奥密克戎BA.2、BA.2.12.1、BA.4/5[8]以及BF.7[9]具有良好的抗病毒活性,适用于目前新冠病毒感染的抗病毒治疗。对于未来可能出现的变异毒株,可以进一步观测其有效性。
END
参考文献:
[1] 《新型冠状病毒感染诊疗方案(试行第十版)》(http://www.nhc.gov.cn/xcs/zhengcwj/202301/32de5b2ff9bf4eaa88e75bdf7223a65a.shtml)
[2] 安巴韦单抗注射液说明书/罗米司韦单抗注射液说明书(2021年12月8日)
[3] Danziger-Isakov L, et al. Am J Transplant. 2021 Mar;21(3):925-937.
[4] Esperança-Martins M, et al. Oncologist. 2021 Sep;26(9):e1619-e1632.
[5] Jang YR, et al. Open Forum Infect Dis. 2022 May 9;9(7):ofac237.
[6] Peter C Taylor, et al. Nat Rev Immunol. 2021;21(6):382-393.
[7] Hoy SM. Drugs. 2022 Aug;82(12):1327-1331.
[8] Ji Y, et al. Front Immunol. 2022 Sep 14;13:980435.
[9] Wang Q, et al. Lancet Infect Dis. 2022 Dec;22(12):1666-1668.
[10] 奈玛特韦片/利托那韦片使用说明书
[11] Hao X, et al. Front Pharmacol. 2022 Sep 6;13:983505.
[12] Qin X, et al. BMC Immunol. 2021 Feb 17;22(1):14.
[13] 中国疾病预防控制中心报告:全国新型冠状病毒感染疫情情况(https://www.chinacdc.cn/jkzt/crb/zl/szkb_11803/jszl_13141/202302/t20230201_263576.html)
[14] 湖北省疾病预防控制中心(https://www.hbcdc.com/xwdt/rdxw/9495.htm)
来源:中国医学论坛报https://mp.weixin.qq.com/s/bSxSuY_YoLbQPZ4x_R3bTw